Состав хрящевой ткани. Хрящевая ткань: функции и особенности строения. Волокнистая ткань: некоторые особенности
Не секрет, что спортсмены даже в хорошей физической форме и в сравнительно раннем возрасте часто бросают тренировки из-за травм. Большая доля их проблем - связки. Наиболее слабая их часть - хрящевая ткань. Функции поврежденных суставов, оказывается, можно восстанавливать, если вовремя обратить внимание на проблему и создать подходящие условия для лечения и регенерации их клеток.
Ткани в организме человека
Человеческий организм - это сложная и гибкая система, способная к саморегулированию. Состоит она из различных по строению и выполняемым функциям клеток. В них происходит основной обмен веществ. Вместе с неклеточными структурами они объединены в ткани: эпителиальная, мышечная, нервная, соединительная.
Эпителиальные клетки составляют основу кожного покрова. Они выстилают внутренние полости (брюшную, грудную, верхние дыхательные пути, кишечный тракт). Мышечная ткань дает возможность человеку двигаться. Также она обеспечивает перемещение внутренних сред во всех органах и системах. Мускулатура подразделяется на виды: гладкая (стенки полостных органов и сосудов), сердечная, скелетная (поперечнополосатая). Нервная ткань обеспечивает передачу импульсов от мозга. Некоторые клетки способны расти и размножаться, часть из них способны к регенерации.
Соединительная ткань является внутренней средой организма. Она различна по структуре, строению и свойствам. Из нее состоят прочные кости скелета, жидкие среды: кровь и лимфа. К ней также относится и хрящевая ткань. Функции ее - формирующая, амортизационная, поддерживающая и опорная. Все они играют важную роль и являются необходимыми в сложной системе организма.
строение и функции
Ее характерная черта - рыхлость в расположении клеток. Рассматривая их по отдельности, можно заметить, как четко отделены они друг от друга. Связкой между ними выступает межклеточное вещество - матрикс. Причем у разных видов хрящей оно образовано кроме основного аморфного вещества различными волокнами (эластичными и коллагеновыми). Хотя они имеют общее белковое происхождение, но различаются по свойствам и в зависимости от этого выполняют различные функции.

Все кости организма сформировались из хрящей. Но по мере роста их межклеточное вещество заполнилось кристаллами солей (в основном кальция). В результате кости приобрели прочность и стали частью скелета. Хрящи также выполняют опорные функции. В позвоночнике, находясь между сегментами, они воспринимают постоянные нагрузки (статические и динамические). Ушные раковины, нос, трахея, бронхи - в этих участках ткань играет больше формирующую роль.
Рост и питание хряща осуществляются через надхрящницу. Она в ткани является обязательной частью, кроме суставов. В них между трущимися поверхностями присутствует синовиальная жидкость. Она омывает, смазывает и питает их, отводит продукты обмена.
Структура
В хряще мало клеток, способных к делению, и много пространства вокруг них, заполненного различным по свойствам белковым веществом. Из-за такой особенности процессы регенерации часто в большей мере идут именно в матриксе.
Выделяют два вида клеток ткани: ходнроциты (зрелые) и хондробласты (молодые). Различаются они размерами, местом и способом расположения. Хондроциты имеют округлую форму, и они крупнее. Располагаются парами или в группах до 10 клеток. Хондробласты обычно мельче и находятся в ткани по периферии или же одиночно.
В цитоплазме клеток под оболочкой накапливается вода, имеются включения гликогена. Кислород и питательные вещества поступают в клетки диффузно. Там происходит синтез коллагена и эластина. Они необходимы для формирования межклеточного вещества. От его специфики зависит, какого типа это будет хрящевая ткань. Особенности строения и отличаются от межпозвоночных дисков, в том числе и содержанием коллагена. В в хряще носа межклеточное вещество состоит на 30 % из эластина.

Виды
Как классифицируется Функции ее зависят от преобладания в матриксе специфических волокон. Если в межклеточном веществе больше эластина, то хрящевая ткань будет более пластична. Она почти такая же прочная, но пучки волокон в ней тоньше. Они хорошо выдерживают нагрузки не только на сжатие, но и на растяжение, способны к деформациям без критических последствий. Такие хрящи называют эластическими. Их ткани формируют гортань, ушные раковины, нос.
Если в матриксе вокруг клеток большое содержание коллагена со сложной структурой построения полипептидных цепей, такой хрящ называют гиалиновым. Он чаще всего покрывает внутренние поверхности суставов. Наибольшее количество коллагена сосредоточено в поверхностной зоне. Он играет роль каркаса. Пучки волокон в нем по структуре напоминают трехмерные переплетенные сети спиралевидной формы.
Есть еще одна группа: фиброзные, или волокнистые, хрящи. Они, как и гиалиновые, содержат в межклеточном веществе большое количество коллагена, но он имеет особую структуру. Пучки их волокон не имеют сложного переплетения и расположены вдоль оси наибольших нагрузок. Они более толстые, имеют особую прочность на сжатие, плохо восстанавливаются при деформации. Из такой ткани сформированы межпозвоночные диски, места стыка сухожилий с костями.

Функции
Благодаря особенным биомеханическим свойствам ткань хряща идеально подходит для связывания составляющих опорно-двигательного аппарата. Она способна принимать воздействие сил сжатия и растяжения при движениях, перераспределять их равномерно нагрузке, до некоторой степени поглощать или рассеивать.
Хрящи образуют устойчивые к истиранию поверхности. В совокупности с синовиальной жидкостью такие суставы при допустимых нагрузках способны продолжительное время нормально выполнять свои функции.
Сухожилия - это не хрящевая ткань. Функции их также заключаются в связывании в общую аппарата. Они также состоят из пучков коллагеновых волокон, но их структура и происхождение другие. органов дыхания, ушных раковин кроме того что выполняют формирующую и опорную функции являются местом крепления мягких тканей. Но в отличие от сухожилий мышцы рядом с ними не имеют такой нагрузки.
Особые свойства
В эластических хрящах очень мало сосудов. И это объяснимо, ведь сильная динамическая нагрузка способна их повредить. Как же питается хрящевая соединительная ткань? Функции эти берет на себя межклеточное вещество. В гиалиновом хряще вообще нет сосудов. Их трущиеся поверхности довольно жесткие и плотные. Питание их осуществляется за счет синовиальной жидкости сустава.
В матриксе вода перемещается свободно. Она содержит все необходимые вещества для обменных процессов. Протеогликановые компоненты в хрящах идеально связывают воду. Она как несжимаемая субстанция обеспечивает жесткость и дополнительную амортизацию. При нагрузках вода принимает на себя воздействие, растекается по всему межклеточному пространству и плавно снимает напряжение, препятствуя необратимым критическим деформациям.

Развитие
В теле взрослого человека до 2 % массы приходится на хрящевую ткань. Где она сосредоточена и какие функции выполняет? Хрящевая и костная ткань в эмбриональном периоде не дифференцируется. У зародышей костей нет. Они развиваются из хрящевой ткани и образуются к моменту рождения. Но часть ее так и не окостеневает. Из нее образуются уши, нос, гортань, бронхи. Также она присутствует в суставах рук и ног, сочленениях межпозвоночных дисках, менисках коленей.
Развитие хряща происходит в несколько этапов. Сначала клетки мезенхимы насыщаются водой, округляются, утрачивают отростки и начинают продуцировать вещества для матрикса. После этого происходит их дифференцировка на хондроциты и хондробласты. Первые оказываются плотно окруженными межклеточным веществом. В таком состоянии они могут делиться ограниченное количество раз. После таких процессов образуется изогенная группа. Клетки, оставшиеся на поверхности ткани, становятся хондробластами. В процессе продуцирования веществ матрикса происходит окончательная дифференцировка, формируется структура с отчетливым делением на тонкую кайму и основу ткани.

Возрастные изменения
Функции хрящевой в процессе жизни не меняются. Однако со временем можно заметить признаки старения: ослабевают мышцы и сухожилия суставов, теряется гибкость, беспокоят боли на перемену погоды или при непривычной нагрузке. Такой процесс считается физиологической нормой. К возрасту 30-40 лет симптомы изменений могут в большей или меньшей степени уже начинать причинять неудобства. Старение ткани суставного хряща происходит из-за потери его эластичности. Теряется упругость волокон. Ткань высыхает, разрыхляется.
На гладкой поверхности появляются трещинки, она становится шероховатой. Плавность и легкость скольжения уже невозможна. Поврежденные края разрастаются, в них образуются отложения, в ткани формируются остеофиты. Эластические хрящи стареют с накоплением в межклеточном веществе кальция, но на их функциях (нос, ушные раковины) это почти не отражается.

Нарушение функции хрящевой и костной ткани
Когда и как это может произойти? В большой степени это зависит от того, какую функцию выполняет хрящевая ткань. В межпозвоночных дисках, основная функция которых стабилизирующая и опорная, чаще всего нарушение работы происходит при развитии дистрофических или дегенеративных процессов. Ситуация может привести к смещениям, что, в свою очередь, повлечет сдавливание окружающих тканей. Неизбежен отек, ущемление нервов, сдавливание сосудов.
Чтобы восстановить стабильность, организм пытается бороться с проблемой. Позвонок в месте деформации «подстраивается» под ситуацию, разрастается в виде своеобразных костных выростов (усов). Это также не идет на пользу окружающим тканям: снова отек, ущемление, сжатие. Такая проблема имеет комплексный характер. Нарушения функционирования костно-хрящевого аппарата принято называть остеохондрозом.
Длительное ограничение движения (гипс при травмах) также негативно сказывается на хрящах. Если при чрезмерных нагрузках эластические волокна перерождаются в грубые фиброзные пучки, то при низкой активности хрящи перестают нормально питаться. Синовиальная жидкость плохо перемешивается, хондроциты недополучают питательные вещества, в результате не вырабатывается необходимое количество коллагена и эластина для матрикса.
Вывод напрашивается сам: для нормальной работы суставов хрящи должны получать достаточную нагрузку на растяжение и сжатие. Чтобы это обеспечить, нужно заниматься физическими упражнениями, вести здоровый и активный образ жизни.
Классификация хрящевых тканей основана на особенностях строения его межклеточного вещества - матрикса. Такая классификация видов хрящевой ткани далеко не совершенна, поскольку не содержит в себе общего единого принципа. Так, термин «фиброзный» указывает на содержание волокнистых структур, а термин «эластический» - уже на определенную конкретную характеристику белка - эластина, входящего в состав хряща. Термин «гиалиновый» информирует лишь о том, что матрикс хряща внешне однородный, а о структуре и характере белков, составляющих его структуру, вообще не упоминается.
).
Хрящевая ткань присутствует во внескелетных образованиях - гортани, носовых перегородках, бронхах, стромальных компонентах сердца.
Внеклеточный матрикс хрящевой ткани отличается от матрикса других разновидностей соединительной ткани существенными особенностями своих структурных макромолекулярных компонентов. Эти особенности обусловливают выраженное своеобразие архитектоники матрикса и его уникальные функциональные (биомеханические) характеристики.
Волокнистые структуры матрикса образованы особыми, специфическими для хрящевой ткани коллагеновыми белками - «большим» фибриллярным коллагеном II типа и сопутствующими ему «малыми» (минорными) коллагенами IX, XI, а также X и некоторых других типов. Главным компонентом межуточного вещества матрикса является также специфический для хрящевой ткани «большой» протеогликан агрекан, макромолекулы которого образуют огромные (их размеры превышают размеры клеток), занимающие большое пространство агрегаты. В состав макромолекул агрекана, составляя значительную часть их массы, входят сульфатированные гликозаминогликаны - хондроитинсульфаты и кератансульфат.
Клетки хрящевой ткани
Дифферон хрящевой ткани может быть представлен следующим образом: прехондробласты-хондробласты-хондроциты. Опираясь на описание дифферона клеток хрящевых тканей, а также из дидактических соображений, мы опишем три формы хондроцитов: прехондробласты, хондробласты и хондроциты.
Прехондробласты
В диффероне хрящевых клеток выделяют клетки-предшественники хондробластов - прехондробласты. Выделение прехондробластов в определенной мере является условным, так как предполагают, что у хряща и кости имеются единые полустволовые клетки - общие для хондробластов и остеобластов.
Хондробласты
Основные процессы формирования хрящевой ткани происходят в эмбриогенезе, где хондроцит функционирует в качестве своей бластной формы и называется хондробластом. По-видимому, целесообразно говорить о единой популяции клеток хондробласт-хондроцит, которая обеспечивает как формирование хрящевой ткани, так и функционирование ее в зрелом состоянии. Источником пополнения популяции таких клеток являются прехондробласты.
Хондробласт можно определить как клетку, находящуюся в стадии перехода от прехондробласта к зрелому хондроциту. Такая клетка обладает секреторными потенциями, необходимыми для синтеза компонентов матрикса, но сохраняет еще способность к пролиферации. Многие исследователи отмечают, что хондробласт и хондроцит не имеют отчетливых морфологических различий, т.е. в морфологической характеристике хондробластов и хондроцитов еще не удалось определить ту меру специфичности, которая позволила бы уверенно различать эти два типа клеток.
Роль хондробластов-хондроцитов как, возможно, единственной клетки в жизнедеятельности хряща настолько важна, что их назвали «архитекторами хряща». Это название отражает тот факт, что она является единственным продуцентом всех макромолекулярных компонентов матрикса хрящевой ткани. Формирование хряща происходит преимущественно в эмбриогенезе и заканчивается в очень молодом возрасте. Таким образом, этот процесс почти целиком происходит на хондробластической стадии дифференцировки клетки.
Хондроциты
Хондроциты - это высокоспециализированная и метаболически активная клетка. Синтетическая деятельность хондроцита специфична и дифференцирована в направлении продукции и секреции коллагена II типа, минорных коллагенов, агрекана, характерных для хрящевой ткани гликопротеинов, эластина (в эластических хрящах). Ультраструктура зрелого хондроцита соответствует высокому уровню его метаболической активности.
Тот факт, что хондроциты служат источником коллагена хрящевой ткани, документируется и биохимическими, и морфологическими методами. Хондроциты в монослойной клеточной культуре дают внутриклеточную иммунофлюоресценцию с сывороткой, меченной к коллагену II типа. Таким же методом удалось локализовать коллаген II типа внутри клеток хрящевой метафизарной пластинки у детей на биопсийном материале.
Не менее убедительны и данные, относящиеся к синтезу протеогликанов. В хондроцитах при ТЭМ выявляются окрашиваемые рутениевым красным гранулы, которые заполняют весь внеклеточный матрикс хрящевой ткани и представляют собой не что иное, как уплотненные в процессе фиксации агрегаты протеогликанов. Эти гранулы обнаруживаются в везикулах комплекса Гольджи, но они отсутствуют в ГЭС. Это означает, что агрекан приобретает свой полианионный характер (рутениевый красный окрашивает полианионные макромолекулы избирательно) при прохождении через комплекс Гольджи. Эти данные согласуются с результатами радиоавтографических исследований, в которых показано, что S35 избирательно концентрируется в комплексе Гольджи. Таким образом, был не только установлен факт биосинтеза хондроцитами агрекана, но и выявлена точная внутриклеточная локализация центрального звена процесса его биосинтеза.
Сопоставление габаритов хондроцита и агреканового агрегата (первый значительно меньше по занимаемому объему, чем второй) позволило заключить, что внутри хондроцита происходит только синтез мономерных макромолекул агрекана, которые секретируются за пределы клетки в матрикс, где и происходит сборка агрекановых агрегатов.
Синтез хондроцитами тканевых структурных гликопротеинов хрящевой ткани доказан биохимическими методами. Получить морфологические подтверждения этого синтеза трудно. Полагают, что он маскируется выраженными процессами синтеза коллагена и протеогликанов. Способность хондроцитов к синтезу белка эластина была показана при исследовании культивируемых хондроцитов ушной раковины кролика.
Согласно современным представлениям, процесс обызвествления хряща происходит при активном участии в нем хондроцитов. Минерализации предшествуют изменения - как в матриксе, так и в клетках хряща.
Гетерогенность хондроцитов
Хондроциты нормальной хрящевой ткани фенотипически представляют собой гетерогенную популяцию клеток.
В гиалиновом хряще выявляются разные по своим морфологическим и функциональным характеристикам хондроциты. Основными являются три их разновидности.
Хондроциты I типа - относительно немногочисленные клетки с неровными отростчатыми краями, крупным ядром, относительно слабо выраженным ГЭС. Клеткам этого типа, например, в суставном хряще, приписывается возможность митотического деления, т.е. функции, необходимой для осуществление физиологической регенерации в процессе естественной смены популяции хондроцитов.
Хондроциты II типа составляют основную массу клеток и характерны для любой разновидности гиалинового хряща. Такой хондроцит - клетка (15- 20 мкм в диаметре) с крупным ядром и многими мелкими отростками, так называемыми цитоплазматическими «ножками». Ядерный хроматин частично конденсирован и сосредоточен в основном на внутренней поверхности ядерной мембраны. В цитоплазме хорошо развита ГЭС, ее каналы местами расширены и наполнены продуктами синтеза. Комплекс Гольджи всегда хорошо развит. Митохондрии немногочисленны.
Хондроциты III типа - это также высокодифференцированные клетки.
Фенотип хондроцита и закономерности его поддержания
Вопрос о том, каковы возможности и необходимые условия для поддержания фенотипа хондроцита в зрелом хряще в норме и при экстремальных ситуациях, являлся в последние годы предметом как изучения, так и дискуссий. Хондроцит и окружающий его матрикс представляют собой единое в функциональном отношении целое - хондроцит продуцирует матрикс, матрикс обеспечивает поддержание фенотипа хондроцита. Соответственно в нормальном хряще in vivo имеются условия, обеспечивающие поддержание стабильности фенотипа хондроцита.
Полагают, что фенотип хондроцита более лабилен, чем фенотип других клеток соединительной ткани. Он приобретается на определенном этапе хондрогенной дифференцировки мезенхимальных клеток и утрачивается в условиях патологии, что, несомненно, имеет патогенетическое значение. Утрата фенотипа хондроцитов происходит также после изолирования их из хрящевой ткани для последующего культивирования в условиях монослойной клеточной культуры. В этом случае на фоне выраженной пролиферации хондроцитов наблюдается угнетение биосинтеза хрящевого матрикса. Этот феномен обычно называют процессом дедифференциации.
Однако при определенных условиях фенотип хондроцитов (например, после перенесения клеток из монослойной в суспензионную культуру) может быстро восстанавливаться. Происходит редифференциация, при которой активируется ряд генов, участвующих в процессе дифференцировки клеток, в том числе гены, кодирующие компоненты системы передачи сигналов одного из цитокинов - IL-6. Напротив, экспрессия некоторых других генов угнетается. В частности, угнетение затрагивает ген фактора роста соединительной ткани (CTGF). Главным признаком редифференциации является возобновление экспрессии специфических компонентов экстрацеллюлярного матрикса, хотя при этом могут частично сохраняться как появившаяся при дедифференциации экспрессия неспецифических продуктов биосинтеза, в частности, коллагена I типа, так и измененная структура хондроцита.
Для поддержания фенотипа зрелого хондроцита необходимо присутствие нормального полноценного хрящевого матрикса. В норме именно структурные особенности матрикса стабилизируют фенотип клеток. Это заключение подтверждается тем фактом, что при культивировании срезов хряща, т.е. при сохранении матрикса, фенотип хондроцитов не изменяется на протяжении длительного времени культивирования (до 9 недель). В условиях патологии фенотип хондроцита изменяется, а задачей терапии является его восстановление.
Метаболические процессы в клетках хрящевой ткани
Хондроциты, как было указано выше, - это единственная разновидность клеток, представленная в зрелой хрящевой ткани, и именно поэтому только они могут служить источником для формирования внеклеточного матрикса. Продукция матрикса и поддержание его структурной целостности на протяжении жизни организма - основные функции хондроцитов. Именно хондроциты осуществляют биосинтез всех специфических компонентов матрикса. Кроме того, хондроциты контролируют протекающие в матриксе процессы сборки надмолекулярных структур (например, агрегатов агрекана и коллагеновых фибрилл) и течение катаболических реакций.
Как мы уже подчеркивали, численность хондроцитов относительно невелика. Они могут обеспечить формирование матрикса только за счет высокой метаболической (анаболической и катаболической) активности каждой клетки. Эта активность, наиболее выраженная в эмбриональном и раннем постнатальном онтогенезе, является одним из характерных свойств хондроцитов.
Метаболическая активность хондроцитов, за исключением общих для всех клеток процессов, обеспечивающих их собственную жизнедеятельность, направлена на построение и поддержание матрикса. Ее целесообразно рассмотреть после того, как будет представлена характеристика структурных компонентов матрикса и действующих в нем ферментов. Здесь мы лишь обратим внимание на те условия, в которых осуществляются метаболические функции хрящевых клеток.
Относительно немногочисленные клетки хрящевой ткани (хондробласты-хондроциты) должны обеспечить образование и последующее поддержание в состоянии динамического равновесия больших масс экстрацеллюлярного матрикса. Свою задачу клетки хряща выполняют в особых условиях: они функционируют в ткани, бедной кровеносными сосудами, а в суставных хрящах взрослых организмов - в бессосудистой ткани. Если хрящи других локализаций, например межреберные, получают необходимые для метаболизма материалы из капилляров надхрящницы (перихондрия), то в суставном хряще, лишенном перихондрия и отделенным пограничной линией от субхондральной кости, возможности получения этих материалов из крови отсутствуют.
Это означает, что в зрелом суставном хряще хондроциты, удаленные от кровеносных сосудов, получают исходные материалы для метаболических процессов только из омывающей суставную поверхность СЖ за счет их проникновения сквозь толщу матрикса. Физическим механизмом, осуществляющим такое проникновение, является диффузия - перемещение находящихся в растворе молекул из области с более высокой концентрацией в область более низкой концентрации до достижения равномерного распределения молекул растворенного вещества среди молекул растворителя.
Скорость диффузии между полярными и неполярными молекулами отчетливо различается. Но интенсивность диффузии всех низкомолекулярных веществ вполне достаточна для того, чтобы обеспечить метаболические потребности хондроцитов по всей толщине суставного хряща, даже в наиболее массивных участках хрящей тазобедренного сустава человека, где толщина хряща достигает 3,5-5 мм. Исключение составляет кислород; его концентрация в СЖ очень низкая. При реально существующей в синовии концентрации кислорода (3-10 х Ю-8 моль/мл) диффузия обеспечивает проникновение кислорода только до глубины около 1,8 мм. Клетки, расположенные в более удаленных от суставной поверхности слоях хряща, оказываются в условиях дефицита кислорода. Вследствие этого метаболические процессы в хондроцитах различных слоев хряща протекают с неодинаковой активностью. Это - еще одно проявление метаболической неоднородности суставных хрящей.
Метаболизм хондроцитов носит преимущественно анаэробный характер, ибо он осуществляется за счет гликолиза. Такая особенность энергетического обеспечения ткани хряща - приспособительный механизм, позволяющий клеткам функционировать в условиях очень низких концентраций кислорода. Если в межклеточных пространствах мягких тканей парциальное давление кислорода составляет 15-20 мм рт. ст., то в суставном хряще оно не превышает 5-8 мм рт. ст. При этом в базальной зоне хряща оно примерно в 10 раз ниже, чем в поверхностных. Чем ниже концентрация кислорода в матриксе хряща, тем выше интенсивность гликолиза и соответственно - продукция молочной кислоты.
Хондроциты фенотипически адаптированы к анаэробным условиям функционирования. Эксперименты in vitro показали, что по мере повышения степени гипоксии анаболические процессы не только не угнетаются, но даже активируются. Повышается эффективность утилизации глюкозы, что обеспечивает более экономное расходование энергии. Однако при слишком выраженной тканевой гипоксии (такое состояние наблюдается при РА, когда очень резко падает содержание кислорода в СЖ) происходит угнетение экспрессии хондроцитами ряда генов. Уровни мРНК, кодирующих структурные макромолекулы матрикса (коллаген II типа), количество некоторых цитокинов и интегринов в хондроцитах при этом снижается.
В то же время в отличие от клеток других тканей хондроциты дают парадоксальную реакцию на увеличение парциального давления кислорода: угнетением биосинтетических процессов, в частности снижением биосинтеза ДНК и протеогликанов. С возрастом потребление кислорода хондроцитами еще более снижается. Потребление кислорода хондроцитами, особенно поверхностного слоя хряща, понижается при избыточной концентрации глюкозы в СЖ.
Биомеханические свойства хряща
Суставные хрящи выполняют две основные биомеханические функции:
- принимают на себя действие сил сжатия (компрессии), обусловленных тяжестью и развивающимися при движениях нагрузками, способствуя их равномерному распределению и переводу аксиально направленных сил в тангенциальные;
- образуют устойчивые к износу поверхности сочленяющихся элементов скелета.
Поскольку хрящевая ткань содержит очень мало клеток - около 1 % массы ткани, эти свойства практически полностью зависят от внеклеточного матрикса.
С точки зрения биомеханики матрикс хрящевой ткани представляет собой материал, состоящий из двух различных фаз - твердой и жидкой. Твердая фаза включает в себя неволокнистые структурные макромолекулы, в числе которых преобладают агрегаты агрекана и волокнистые структурные макромолекулы, среди которых преобладает коллаген II типа. Жидкая фаза составляет примерно 80 % массы ткани.
Коллагеновые волокна образуют прочную сеть, которая фиксирует агрегаты агрекана и, ограничивая в пространстве отрицательно заряженные макромолекулы агрекана, не позволяет им распространиться в максимальном объеме. Эта сеть (каркас) мало растяжима и обеспечивает прочность хряща на разрыв.
Композитная твердая фаза матрикса функционирует как пористый, проницаемый, скрепленный волокнами материал, набухший водой. Молекулы воды располагаются внутри пространств, занимаемых диффузными агрегатами агрекана, и именно вода, как несжимаемая жидкость, обеспечивает прочность хряща на сжатие. Протеогликановый компонент матрикса, в силу своих полианионных свойств, ответствен за гипергидратированное состояние хряща и, следовательно, играет определяющую роль в формировании прочности к сдавливающим нагрузкам. Существует выраженная положительная корреляция между концентрацией в хряще агрекана и его прочностью на сжатие.
Только менее 1 % молекул воды прочно удерживается коллагеновыми волокнами. Остальные (более 99%) молекулы воды, располагающиеся в межволокнистой субстанции матрикса, достаточно свободны и подвижны. При компрессионных нагрузках эти свободные молекулы вместе с растворенными в воде низкомолекулярными веществами могут перемещаться по матриксу и «выжиматься» из хряща в СЖ. При уменьшении давления происходит движение в обратном направлении - из СЖ в матрикс. Этим объясняется способность хряща к обратимой деформации (упругость).
При движении воды в пористом материале, каким является матрикс, возникает трение, которое в сочетании с некоторыми особенностями твердой фазы (в основном речь идет о сложной системе межмолекулярных связей компонентов матрикса) обусловливает определенную вязкость хрящевой ткани.
Таким образом, двухфазная модель в целом объясняет вязкоупругие биомеханические свойства хряща. Вместе с тем она встречает и возражения. Главное из них - неправомерность объединения всех твердых компонентов в одну фазу. Эксперименты N.D. Broom, Н. Silyn-Roberts показали, что разрушение значительной части агрекановых агрегатов (с помощью гиалуронидазы) практически не отражается на прочности хряща на разрыв и, следовательно, коллагеновые волокна в этой биомеханической функции независимы от агрекана. Вероятно, укрепление коллагеновых волокон за счет взаимодействия коллагенов различных типов более существенно, чем связи между коллагенами и агреканом, поэтому появляются основания рассматривать агрекан и коллагены как две отдельные фазы, что означает переход к трехфазной биомеханической модели хряща (коллагены-агрекан-вода).
Вполне возможно, что на биомеханических свойствах хряща сказывается влияние гликопротеинов. Это означает, что и трехфазная модель недостаточно учитывает всю многокомпонентность хрящевого матрикса. Но независимо от того, какая биомеханическая модель окажется окончательной, очевидно, что нормальное функционирование хряща возможно только при оптимальных количественных и структурных взаимоотношений всех компонентов матрикса.
Они выполняют механическую, опорную, защитную функции. В них упругое плотное межклеточное вещество. Содержание воды до 70-80%, минеральных веществ до 4-7%, органические вещества составляют до 10-15%, и в них преобладают белки, углеводы и крайне мало липидов. В них выделяются клетки и межклеточное вещество. Клеточный состав всех разновидностей хрящевых тканей одинаковый и включает хондробласты – малодифференцированные, уплощнные клетки с базофильной цитоплазмой, они способны пролиферировать и вырабатывать межклеточное вещество. Хондробласты дифференцируются в молодые хондроциты, приобретают овальную форму. Они сохраняют способность к пролиферации и выработке межклеточного вещества. Затем малые дифференцируются в более крупные, округлые зрелые хондроциты. Они утрачивают способность к пролиферации и выработке межклеточного вещества. Зрелые хондроциты в глубине хряща скапливаются в одной полости и называются изогенными группами клеток.
Отличаются хрящевые ткани строением межклеточного вещества и волокнистыми структурами. Различают гиалиновую, эластическую и волокнистую хрящевые ткани. Они участвуют в образовании хрящей и образуют гиалиновый, эластический и волокнистый хрящ.
Гиалиновый хрящ выстилает суставные поверхности, находится в зоне соединения рёбер с грудиной и в стенке воздухоносных путей. Снаружи покрыт надхрящницей – перихондрий, который содержит кровеносные сосуды. Е периферическая часть состоит из более плотной соединительной ткани, а внутренняя часть из рыхлой, содержит фибробласты и хондробласты. Хондробласты вырабатывают и выделяют межклеточное вещество и обусловливают аппозиционный рост хряща. В периферической части собственно хряща находятся молодые хондроциты. Они пролиферируют, вырабатывают и выделяют хондромукой (хондроитинсульфаты + протеогликаны), обеспечивая рост хряща изнутри.
В средней части хряща находятся зрелые хондроциты и изогенные группы клеток. Между клетками располагается межклеточное вещество. Оно содержит основное вещество и коллагеновые волокна. Сосуды отсутствуют, питается он диффузно из сосудов надкостницы. В молодом хряще межклеточное вещество оксифильное, постепенно становится базофильным. С возрастом, начиная с центральной части, в нм откладываются соли кальция, хрящ обызвествляется, становится хрупким, ломким.
Эластический хрящ – образует основу ушной раковины, в стенке воздухоносных путей. Он аналогичен по строению гиалиновому хрящу, но содержит не коллагеновые, а эластические волокна, и в норме он никогда не обызвествляется.
Волокнистый хрящ – он находится в зоне перехода связок, сухожилий с костной тканью, в участке, где кости покрыты гиалиновым хрящом и в зоне межпозвоночных соединений. В нем грубые пучки коллагеновых волокон идут продольно оси натяжения, являясь продолжением сухожильных нитей. Волокнистый хрящ в области прикрепления к кости больше похож на гиалиновый хрящ, а в области перехода в сухожилие – на сухожилие.
⇐ Предыдущая1234
Питание хрящевой ткани идет путем диффузии веществ из кровеносных сосудов надхрящницы. В ткань суставных хрящей питательные вещества проникают из синовиальной жидкости или из сосудов прилегающей кости.
Хрящевая ткань: функции, особенности строения, виды, восстановление
Нервные волокна также локализуются в надхрящнице, откуда отдельные ответвления безмякотных нервных волокон могут проникать внутрь хрящевой ткани.
Гиалиновый хрящ
Эластический хрящ
Волокнистый хрящ
Функции костных тканей:
1) опорная;
2) механическая;
остеоциты . Это клетки отростчатой формы с крупным ядром и слабо выраженной цитоплазмой (клетки ядерного типа). Тела клеток локализуются в костных полостях (лакунах), а отростки – в костных канальцах. Многочисленные костные канальцы, анастомозируя между собой, пронизывают костную ткань, сообщаясь периваскулярным пространством, образуют дренажную систему костной ткани. В этой дренажной системе содержится тканевая жидкость, посредством которой обеспечивается обмен веществ не только между клетками и тканевой жидкостью, но и в межклеточном веществе.
Остеобласты
Остеокласты
Межклеточное вещество
Кость
Классификация костных тканей
⇐ Предыдущая1234
Похожая информация:
- Взаимное расположение прямых.
Поиск на сайте:
Хрящевая ткань- строение, виды, расположение в организме.
⇐ Предыдущая1234
Хрящевая ткань (textus cartilaginus) образует суставные хрящи, межпозвоночные диски, хрящи гортани, трахеи, бронхов, наружного носа. Состоит хрящевая ткань из хрящевых клеток (хондробластов и хондроцитов) и плотного, упругого межклеточного вещества.
Хрящевая ткань содержит около 70-80 % воды, 10-15 % органических веществ, 4-7 % солей. Около 50-70 % сухого вещества хрящевой ткани — это коллаген. Межклеточное вещество (матрикс), вырабатываемое хрящевыми клетками, состоит из комплексных соединений, в которые входят протеогликаны. гиалуроновая кислота, молекулы гликозаминогликанов. В хрящевой ткани присутствуют клетки двух типов: хондробласты (от греч. chondros — хрящ) и хондроциты.
Хондробласты — это молодые, способные к митотическому делению округлые или овоидные клетки. Они продуцируют компоненты межклеточного вещества хряща: протеогликаны, гликопротеины, коллаген, эластин. Цитолемма хондробластов образует множество микроворсинок. Цитоплазма богата РНК, хорошо развитой эндоплазматической сетью (зернистой и незернистой), комплексом Гольджи, митохондриями, лизосомами, гранулами гликогена. Ядро хондробласта, богатое активным хроматином, имеет 1-2 ядрышка.
Хондроциты — это зрелые крупные клетки хрящевой ткани. Они округлые, овальные или полигональные, с отростками, развитыми органеллами. Хондроциты располагаются в полостях — лакунах, окружены межклеточным веществом. Если в лакуне одна клетка, то такая лакуна называется первичной. Чаще всего клетки располагаются в виде изогенных групп (2-3 клетки), занимающих полость вторичной лакуны. Стенки лакуны состоят из двух слоев: наружного, образованного коллагеновыми волокнами, и внутреннего, состоящего из агрегатов протеогликанов, которые входят в контакт с гликокаликсом хрящевых клеток.
Структурной и функциональной единицей хрящей является хондрон, образованный клеткой или изогенной группой клеток, околоклеточным матриксом и капсулой лакуны.
Питание хрящевой ткани идет путем диффузии веществ из кровеносных сосудов надхрящницы. В ткань суставных хрящей питательные вещества проникают из синовиальной жидкости или из сосудов прилегающей кости. Нервные волокна также локализуются в надхрящнице, откуда отдельные ответвления безмякотных нервных волокон могут проникать внутрь хрящевой ткани.
В соответствии с особенностями строения хрящевой ткани различают три вида хряща: гиалиновый, волокнистый и эластический хрящ.
Гиалиновый хрящ
, из которого у человека образованы хрящи дыхательных путей, грудных концов ребер и суставных поверхностей костей. В световом микроскопе основное вещество его представляется гомогенным. Хрящевые клетки или изогенные группы их окружены оксифильной капсулой. В дифференцированных участках хряща различают прилегающую к капсуле базофильную зону и расположенную кнаружи от нее оксифильную зону; в совокупности эти зоны образуют клеточную территорию, или хондриновый шар. Комплекс хондроцитов с хондриновым шаром обычно принимают за функциональную единицу хрящевой ткани - хондрон. Основное вещество между хондронами называют интертерриториальными пространствами.
Эластический хрящ
(синоним: сетчатый, упругий) отличается от гиалинового наличием в основном веществе ветвящихся сетей эластических волокон. Из него построены хрящ ушной раковины, надгортанника, врисберговы и санториновы хрящи гортани.
Волокнистый хрящ
(синоним соединительнотканный) расположен в местах перехода плотной волокнистой соединительной ткани в гиалиновый хрящ и отличается от последнего наличием в основном веществе настоящих коллагеновых волокон.
7.Костные ткань-расположение, строение, функции
Костная ткань является разновидностью соединительной ткани и состоит из клеток и межклеточного вещества, в котором содержится большое количество минеральных солей, главным образом фосфат кальция. Минеральные вещества составляют 70% костной ткани, органические – 30%.
Функции костных тканей:
1) опорная;
2) механическая;
3) защитная (механическая защита);
4) участие в минеральном обмене организма (депо кальция и фосфора).
Клетки костной ткани – остеобласты, остеоциты, остеокласты. Основными клетками в сформированной костной ткани являются остеоциты . Это клетки отростчатой формы с крупным ядром и слабо выраженной цитоплазмой (клетки ядерного типа).
Функции хрящевой ткани
Тела клеток локализуются в костных полостях (лакунах), а отростки – в костных канальцах. Многочисленные костные канальцы, анастомозируя между собой, пронизывают костную ткань, сообщаясь периваскулярным пространством, образуют дренажную систему костной ткани. В этой дренажной системе содержится тканевая жидкость, посредством которой обеспечивается обмен веществ не только между клетками и тканевой жидкостью, но и в межклеточном веществе.
Остеоциты являются дефинитивными формами клеток и не делятся. Образуются они из остеобластов.
Остеобласты содержатся только в развивающейся костной ткани. В сформированной костной ткани они содержатся обычно в неактивной форме в надкостнице. В развивающейся костной ткани остеобласты охватывают по периферии каждую костную пластинку, плотно прилегая друг к другу.
Форма этих клеток может быть кубической, призматической и угловатой. В цитоплазме остеобластов содержатся хорошо развитая эндоплазматическая сеть, пластинчатый комплекс Гольджи, много митохондрий, что свидетельствует о высокой синтетической активности этих клеток. Остеобласты синтезируют коллаген и гликозаминогликаны, которые затем выделяют в межклеточное пространство. За счет этих компонентов формируется органический матрикс костной ткани.
Эти клетки обеспечивают минерализацию межклеточного вещества посредством выделения солей кальция. Постепенно выделяя межклеточное вещество, они как бы замуровываются и превращаются в остеоциты. При этом внутриклеточные органеллы в значительной степени редуцируются, синтетическая и секреторная активность снижается, и сохраняется функциональная активность, свойственная остеоцитам. Остеобласты, локализующиеся в камбиальном слое надкостницы, находятся в неактивном состоянии, синтетические и транспортные органеллы в них развиты слабо. При раздражении этих клеток (в случае травм, переломов костей и т. д.) в цитоплазме быстро развиваются зернистая ЭПС и пластинчатый комплекс, происходит активный синтез и выделение коллагена и гликозаминогликанов, формирование органического матрикса (костной мозоли), а затем и формирование дефинитивной костной ткани. Таким способом за счет деятельности остеобластов надкостницы происходит регенерация костей при их повреждении.
Остеокласты – костеразрушающие клетки, в сформированной костной ткани отсутствуют, но содержатся в надкостнице и в местах разрушения и перестройки костной ткани. Поскольку в онтогенезе непрерывно осуществляются локальные процессы перестройки костной ткани, то и в этих местах обязательно присутствуют и остеокласты. В процессе эмбрионального остеогистогенеза эти клетки играют очень важную роль и присутствуют в большом количестве. Остеокласты имеют характерную морфологию: эти клетки являются многоядерными (3 – 5 и более ядер), имеют довольно крупный размер (около 90 мкм) и характерную форму – овальную, но часть клетки, прилежащая к костной ткани, имеет плоскую форму. В плоской части можно выделить две зоны: центральную (гофрированную часть, содержащую многочисленные складки и отростки, и периферическая часть (прозрачную) тесно соприкасающуюся с костной тканью. В цитоплазме клетки, под ядрами, располагаются многочисленные лизосомы и вакуоли различной величины.
Функциональная активность остеокласта проявляется следующим образом: в центральной (гофрированной) зоне основания клетки из цитоплазмы выделяются угольная кислота и протеолитические ферменты. Выделяющаяся угольная кислота вызывает деминерализацию костной ткани, а протеолитические ферменты разрушают органический матрикс межклеточного вещества. Фрагменты коллагеновых волокон фагоцитируются остеокластами и разрушаются внутриклеточно. Посредством этих механизмов происходит резорбция (разрушение) костной ткани, и потому остеокласты обычно локализуются в углублениях костной ткани. После разрушения костной ткани за счет деятельности остеобластов, выселяющихся из соединительной ткани сосудов, происходит построение новой костной ткани.
Межклеточное вещество костной ткани состоит из основного (аморфного) вещества и волокон, в которых содержатся соли кальция. Волокна состоят из коллагена и складываются в пучки, которые могут располагаться параллельно (упорядоченно) или неупорядоченно, на основании чего и строится гистологическая классификация костных тканей. Основное вещество костной ткани, как и других разновидностей соединительных тканей, состоит из гликозамино– и протеогликанов.
В костной ткани содержится меньше хондроитинсерных кислот, но больше лимонной и других, которые образуют комплексы с солями кальция. В процессе развития костной ткани вначале образуется органический матрикс – основное вещество и коллагеновые волокна, а затем уже в них откладываются соли кальция. Они образуют кристаллы – гидрооксиапатиты, которые откладываются как в аморфном веществе, так и в волокнах. Обеспечивая прочность костей, фосфорнокислые соли кальция являются также одновременно и депо кальция и фосфора в организме. Таким образом, костная ткань принимает участие в минеральном обмене организма.
При изучении костной ткани следует также четко разделять понятия «костная ткань» и «кость».
Кость – это орган, основным структурным компонентом которого являются костная ткань.
Классификация костных тканей
Различают две разновидности костных тканей:
1) ретикулофиброзную (грубоволокнистую);
2) пластинчатую (параллельно волокнистую).
В основе классификации лежит характер расположения коллагеновых волокон. В ретикулофиброзной костной ткани пучки коллагеновых волокон толстые, извилистые и располагаются неупорядоченно. В минерализованном межклеточном веществе в лакунах беспорядочно располагаются остеоциты. Пластинчатая костная ткань состоит из костных пластинок, в которых коллагеновые волокна или их пучки располагаются параллельно в каждой пластинке, но под прямым углом к ходу волокон соседних пластинках. Между пластинками в лакунах располагаются остеоциты, тогда как их отростки проходят в канальцах через пластинки.
В организме человека костная ткань представлена почти исключительно пластинчатой формой. Ретикулофиброзная костная ткань встречается только как этап развития некоторых костей (теменных, лобных). У взрослых людей она находится в области прикрепления сухожилий к костям, а также на месте окостеневших швов черепа (стреловидного шва, чешуи лобной кости).
⇐ Предыдущая1234
Похожая информация:
- I. ВИДЫ, ФОРМЫ И НАПРАВЛЕНИЯ ОРГАНИЗАЦИИ САМОСТОЯТЕЛЬНОЙ РАБОТЫ СТУДЕНТОВ
- II. Виды, условия и формы оказания медицинской помощи
- Артериальное полнокровие. Причины, виды, клинико-морфологическая характеристика.
- Атрофия: причины, механизмы, виды, клинико-морфологическая характеристика. Бурая атрофия печени, миокарда, скелетных мышц.
- Базовой классификацией источников трудового права является их расположениепо юридической силе.
- Бюджетные фонды: понятие, виды, назначение.
- Взаимное расположение поверхностных мышц
- Взаимное расположение прямых.
- Виды, свойства и закономерности эмоций и чувств
- Виды, типы и технико-экономическая характеристика фасовочно-упаковочного оборудования
- Внебюджетные фонды: понятие, виды, порядок и источники их формирования и направления использования. Порядок утверждения отчетов об их исполнении.
- Внешнеэкономическая деятельность. Понятие, виды, субъекты.
Поиск на сайте:
Хрящевая соединительная ткань человека
Одной из разновидностей соединительной ткани, присутствующей в организме человека, является хрящ. Отличается хрящевая соединительная ткань относительно высокой плотностью и упругостью межклеточного вещества, обволакивающего группы хондроцитов и отдельные клетки. От костной ткани (а также от ряда других тканей) хрящ отличается полным отсутствием кровеносных сосудов и нервов. Оболочкой хряща выступает перихондрий, который так же называют надхрящницей. Хрящевая соединительная ткань (ХСТ) может выполнять функцию жесткой скелетной основы у некоторых животных либо формирует упругие участки скелета, покрывая края костей и образуя особые амортизирующие прослойки (как, к примеру, межпозвоночные диски). Словом, основными функциями хрящевой соединительной ткани являются: опорная и функция формирования сочленений.
Строение хрящевой ткани
Как уже отмечалось выше, хрящевая ткань состоит не только из самого хряща, но и из надхрящницы (перихондрия), которая в свою очередь включает внутренний слой рыхлой волокнистой соединительной ткани (РВСТ) и наружный слой плотной волокнистой неоформленной соединительной ткани (ПВНСТ). В состав РВСТ (наряду с хондроцитами и межклеточным веществом, состоящим из волокон, интерстициальной воды и аморфного вещества) входят также полустволовые и стволовые клетки, система кровеносных сосудов, нервы и хондробласты. Объем хондроцитов составляет ориентировочно до 10% от общей массы хрящевой соединительной ткани. Больше всего в ХСТ межклеточного вещества, отличающегося довольно высокой гидрофильностью, а соответственно обеспечивающего возможность доставки в клетки необходимых питательных веществ из кровеносных капилляров перихондрия за счет процессов диффузии. Хрящ может быть стекловидным (в случае однородности межклеточного вещества), волокнистым либо сетчатым.
Хондроциты
Дифферон хондроцитов, из которых состоит хрящевая соединительная ткань, включает хондробласты, стволовые и полустволовые клетки, а также в него входят зрелые и молодые хондроциты. Хондроциты – это производные хондробластов, а кроме того, это клетки, которые единственные из имеющихся в хрящевой ткани клеточных популяций находятся в лакунах. Различают молодые и зрелые хондроциты. Первые во многом идентичны хондробластам. У них продолговатая форма, достаточно большой аппарат Гольджи, а кроме того они могут продуцировать гликопротеины и белок для эластических и коллагеновых волокон. Зрелые клетки-хондроциты овальные по форме и менее способны к синтезу, если проводить сравнение с хондроцитами молодыми. Хондроциты могут делиться и формировать отдельные клеточные группы, обрамленные единой капсулой. В стекловидном хряще могут присутствовать клеточные группы числом до 12 клеток в каждой, а в других типах хрящевой ткани изогенные группы содержат, как правило, меньшее количество клеток.
Хрящевые ткани: классификация и гистогенез
Хрящевая соединительная ткань развивается не только на эмбриональном уровне, но и у взрослых особей (регенерация ткани). В период развития хряща образуется так называемый хрящевой дифферон, в котором последовательно сменяют друг друга стволовые и полустволовые клетки, а затем хондробласты и хондроциты. На первоначальной стадии хрящевого эмбриогенеза формируется небольшой хондрогенный островок. Далее происходит дифференциация хондробластов с последующим появлением хрящевого матрикса и волокон. На завершающей стадии эмбриогенеза хрящевая закладка переживает интерстициальный или аппозиционный рост.
Хрящевые ткани
При первом ткань увеличивается изнутри (свойственно как эмбриональному периоду, так и процессам регенерации), а при втором ткань наслаивается с подачи хондробластов, действующих в перихондрии.
Регенерация и возрастные изменения
Хрящи восстанавливаются за счет глюкозамина и хондроитин сульфата. Эти компоненты являются строительным материалом, благодаря которому происходит восстановление эластичности и структуры суставов, устраняется артрозная боль, восполняется недостающий объем ткани, усиливается действие препаратов противовоспалительного характера. Регенерация хрящевой ткани осуществляется из камбиальных клеток перихондрия (нарастают новые хрящевые слои). Данный процесс может протекать в полную силу лишь в детском возрасте, а у взрослых регенерация хряща, к сожалению, происходит не полностью. В частности, на месте утраченной хрящевой ткани формируется ПВНСТ. С возрастом человека, его волокнистая и эластическая хрящевые ткани не претерпевают практически никаких изменений. В то же время, стекловидный хрящ (гиалиновая хрящевая ткань) склонен к трансформациям в костную ткань и к обызвествлению.
Гиалиновая хрящевая ткань
Стекловидная ткань локализуется преимущественно в хрящах гортани, носа, бронхов, трахеи, ребер, суставов, а также в хрящевых пластинах роста, присутствующих в трубчатых костях. Состоит гиалиновый хрящ из хондроцитов и, соответственно, межклеточного вещества, которое в свою очередь включает коллагеновые волокна, интерстициальную воду и протеогликаны. Примерно 20-25% от общего объема приходится на коллагеновые волокна, а 5-10% на протеогликаны. Последние не допускают минерализации стекловидной хрящевой ткани, а интерстициальная вода, объем которой достигает 65-85%, способствует амортизации хряща и нормальному обмену веществ в соединительной ткани, перенося питательные компоненты, метаболиты и соли. Разновидностью стекловидного хряща является суставной хрящ. Однако при этом он не имеет надхрящницы, а получает необходимые питательные элементы из синовиальной жидкости. В хряще суставном могут быть выделены: бесклеточная зона (поверхностная), промежуточная зона и так называемая глубокая зона, т.е. зона взаимодействия хрящевой ткани с костной.
Эластическая и волокнистая хрящевые ткани
Хрящевая соединительная ткань, называемая эластической, локализуется в рожковидных, надгортанных, черпаловидных (в голосовых отростках) и клиновидных хрящах гортани. Кроме того, эластическая хрящевая ткань встречается в ушной раковине и евстахиевой трубе. Данная разновидность ткани особенно нужна там, где требуется способность участков органов к изменению формы и объема, а также к обратным деформациям. В состав эластической ткани входят хондроциты и состоящее из аморфного вещества (и волокон) межклеточное вещество.
Хрящевая ткань, называемая волокнистой, локализуется в суставных менисках и дисках, межпозвоночных дисках (в их фиброзных кольцах), в лонном сочленении (симфизе), в зонах фиксации сухожилий к гиалиновому хрящу и костям, а кроме того на поверхностях грудинно-ключичного и височно-нижнечелюстного суставов. Волокнистая хрящевая соединительная ткань состоит из удлиненных одиночных хондроцитов и межклеточного вещества. Последнее включает значительное количество волокон коллагена и достаточно малый объем аморфного вещества. Обычно коллагеновые волокна размещены в межклеточном веществе в виде пучков, располагающихся параллельно и упорядоченно.
Виды хрящевой ткани и ее строение
Хрящевая ткань – разновидность упругой, плотной соединительной ткани, имеющей опорно-механическую функцию.
Преимущественный состав хрящевой ткани : хондроциты, хондробласты.
Виды хрящевой ткани
— Гиалиновая (стекловидная) – находится в трубках дыхательных путей, на окончаниях реберных костей и в суставах.
— Волокнистая (соединительнотканная) – служит для соединения плотной ткани с волокнистой структурой гиалинового хряща.
— Эластическая (имеет сетчатую структуру) – содержится в плотных частях ушных раковин, гортани (санториновы, врисберговы, черпаловидный, щитовидный, перстневидный хрящи), надгортаннике.
Функции хрящевой ткани
— Обеспечение надежного соединения с сохранением подвижности между отдельными элементами опорно-двигательного аппарата (например, между костными частями позвоночника);
— Задействование в процессах углеводного обмена.
Полная регенерация хрящевой ткани наблюдается у человека в детском возрасте. С возрастом 100% восстановление невозможно: поврежденные хрящевые ткани восстанавливаются частично, с параллельным формированием на месте травмы ПВНСТ.
При механическом повреждении сустава или если разрушение вызвано следствием болезни, возможна замена сустава на искусственный.
Поддержку естественных функций хрящевой ткани оказывают препараты с хондроитином сульфат натрия, глюкозамином.
Хороший терапевтический эффект на начальных стадиях проблем с хрящевой тканью оказывают умеренные физические упражнения и курс противовоспалительного лечения с одновременным употреблением препаратов с легкоусвояемым кальцием.
Развитие проблем обуславливают:
— травмы,
— инфекционные заболевания,
— чрезмерные физические нагрузки на протяжении длительного периода,
— переохлаждение,
— наследственность.
Положительный эффект от противовоспалительной терапии наблюдается как при приеме препаратов во внутрь, так и при наружном применении. Эффективность последнего метода воздействия основывается на высокой гидрофильности хрящевой ткани. За счет этого проникающие в кожу лекарственные препараты быстро оказываются непосредственно в очаге заболевания.
Все наши кости в процессе эмбрионального (зародышевого) развития образуются из хрящей. У взрослого человека они составляют не более 2% массы тела. Кости растут благодаря диафизарному хрящу, удлиняются они до тех пор, пока не закрываются так называемые зоны роста1. Однако некоторые из них увеличиваются в течение всей жизни человека. Установлено, что постоянно растут, хотя и малыми темпами, нижняя челюсть, нос, ушные раковины, ступни ног и кисти рук.
Наиболее часто, спортсмены покидают спорт из-за травм суставно-связочного аппарата. Его слабое место — хрящ. Проблемы с позвоночником также обусловлены в основном патологией межпозвоночных хрящей.
Можно сказать, что в спортивной травматологии лечение хрящей является заботой № 1. При этом некоторые авторы считают, что восстанавливаются они не более чем на 50%, ставя, таким образом, под сомнение возможность полного восстановления спортивной работоспособности. Попробуем более подробно рассмотреть, что же такое хрящ и определить пределы и методы его регенерации.
Хрящевая ткань — одна из разновидностей соединительной ткани, которая выполняет в организме опорные функции. Непременным атрибутом хряща, за исключением суставного, является надхрящница, обеспечивающая его питание и рост. В суставах хрящ обнажен и контактирует непосредственно с внутренней средой сустава — синовиальной жидкостью. Она выполняет роль своеобразной смазки между трущимися поверхностями суставов, покрытых гладким глиаиновым хрящом. Хрящи костей и позвоночника постоянно испытывают как статическую, так и динамическую нагрузки. Хрящи носа, гортани, бронхов, фиброзных треугольников в сердце осуществляют также и опорную функцию.
Структура хряща позволяет ему испытывать обратимую деформацию и в то же время сохранять способность к обмену веществ и размножению. Главные его компоненты — хрящевые клетки (хендроциты) и внеклеточный матрикс, состоящий из волокон и основного вещества. Причем, большую часть массы хряща составляет именно межклеточное вещество.
В зависимости от преобладания коллагеновых, эластических волокон или основного вещества различают гиалиновый, эластический и волокнистый хрящ.
Особенностью хряща, по сравнению с другими видами тканей в организме является то, что в нем мало клеток и они окружены большим количеством межклеточного пространства — матрикса. Хрящ так плохо восстанавливается после повреждений именно потому, что в нем очень мало клеток, способных размножаться и основная часть репарации (восстановления) идет за счет внеклеточного матрикса. В эластическом хряще (гортани, носа, ушной раковины) содержится много эластина (из него, например, на 30% состоит ухо человека).
В суставном хряще очень много воды (в хряще головки бедренной кости молодого человека — 75 г на 100 г ткани). Глауроновая кислота помогает матриксу связывать воду, чем и обеспечиваются упругие и эластические свойства ткани.
В гиалиновом хряще, который чаще всего представляет внутрисуставную поверхность, половину всего матрикса составляет коллаген — основной белок соединительной ткани. Только сухожилия и дерма (глубокий слой кожи) превосходят матрикс по насыщенности коллагеном. Наибольшая его концентрация в суставных хрящах сосредоточена в поверхностной зоне.
Коллаген — понятие собирательное, существуют несколько его видов. Разные по химическому составу, все они, тем не менее, состоят из очень крупных молекул, свернутых в тройные спирали. Такое строение волокон делает их очень прочными на скручивание, растяжение и разрыв. Каждая из трех цепей имеет полипептидную структуру.
Если мы проанализируем состав полипептидных цепей любого из трех видов коллагена (у человека их насчитывается именно три), то увидим, что наиболее велик удельный вес аминокислоты глицина. Следом за ним по удельному весу следуют аминокислоты промен (пролин -?) и аланин. Иногда аланин «перевешивает» пролин, а иногда наоборот, пролин по своему удельному весу превосходит аланин.
Эластические хрящи (например, носа и ушей) содержат в своем матриксе преимущественно эластин, который, подобно коллагену, формирует прочные волокна. Они тоньше коллагеновых, но отличаются большой прочностью. Ткани, содержащие большое количество эластина способны к очень большим обратимым деформациям. Основной аминокислотой эластина (так же как и коллагена) является глицин. За ним по процентному содержанию следуют аланин, пролин и валин.
Эластина, как и коллагена, существует несколько видов. Волокна эластина тоже имеют пептидный характер и спиралевидную форму. Этим и объясняется их большая растяжимость. Спираль, однако, не тройная, а одинарная, поэтому волокна эластина тоньше коллагеновых. У разных хрящей в матриксе преобладают либо коллагеновые, либо эластиновые волокна. Все они переплетены в прочную трехмерную сеть. Коллагеновая (эластиновая) сеть «удерживает» внутри хряща и другие молекулы как механически, так и с помощью электростатических связей.
Биомеханические свойства хрящей делают их высокоспецифическими и по существу уникальными компонентами опорно-двигательного аппарата.
Они:
а) принимают на себя действие внешних механических сил сжатия и растяжения; распределяют эти силы равномерно, поглощают и рассеивают их, переводя аксиально направленные силы в тангенциальные (в суставах конечностей, позвоночника и т.д.);
б) образуют устойчивые к износу поверхности сочленений скелета, участвуют в формировании смазочного аппарата в синовиальных суставах;
в) являются местом прикрепления и опорой для мягких тканей и мышц; образуют полости в местах контакта с внешней средой (хрящи носа, ушей, органов дыхания).
Считается, что хрящевой матрикс состоит из 3-х основных компонентов:
1) волокнистый коллагеновый каркас, который образует трехмерную сеть переплетений;
2) молекулы протеогликанов, которые заполняют петли волокнистого каркаса;
3) вода, свободно перемещающаяся между переплетениями каркаса и молекулами протеогликанов.
У суставного хряща нет кровеносных сосудов. Он питается диффузно, поглощая питательные вещества из синовиальной жидкости.
Коллагеновый каркас является как бы «скелетом» хряща. Он обладает большой упругостью по отношению к силам растяжения и в тоже время оказывает относительно слабое сопротивление нагрузке на сжатие. Поэтому внутрисуставные хрящи (например: мениски и суставные поверхности бедренной и берцовых костей) легко повреждаются при компрессионных (сжимающих) нагрузках и почти никогда при нагрузках на растяжение («на разрыв»).
Протеогликановый компонент матрикса отвечает за способность хряща связывать воду. Она может удаляться за пределы хряща в синовиальную жидкость и возвращаться в него обратно. Именно вода как несжимаемая субстанция обеспечивает достаточную жесткость хряща. Ее перемещения равномерно распределяет внешнюю нагрузку по всему хрящу, в результате чего происходит ослабление внешних нагрузок и обратимость возникающих при нагрузках деформаций.
Эластические хрящи гортани, трахеи содержат очень небольшое количество сосудов. Коллагеновые хрящи суставов вообще не содержат сосудов. Большая механическая нагрузка на хрящ несовместима с васкуляризацией (сосудистым обеспечением). Обмен в таком хряще осуществляется благодаря перемещению воды между компонентами матрикса. Она содержит все необходимые хрящам метаболиты. Поэтому в них резко замедлены как анаболические, так и катаболические процессы. Отсюда плохое их посттравматическое восстановление, в отличие от хрящей с васкуляризацией.
Кроме глиаинового и эластического хрящей выделяют еще одну группу — волокнистый, или фиброзный хрящ. Фиброз — значит «волокно». Матрикс фиброзного хряща образован коллагеновыми волокнами, однако, по сравнению, скажем, с глиаиновым хрящом пучки коллагеновых волокон более толстые и не имеют структуры трехмерного переплетения. Они ориентированы, в основном, параллельно друг другу. Их направление соответствует векторам сил натяжения и давления. Из фиброзного хряща состоят межпозвонковые диски, отличающиеся большой прочностью. Крупные коллагеновые волокна и их пучки располагаются в межпозвонковых дисках циркулярно. Помимо межпозвонковых дисков волокнистый хрящ находится в местах прикрепления сухожилий к костям или хрящам, а также в сочленении лобковых костей.
Поддержание всей структурной целостности матрикса хряща зависит целиком от хондроцитов. И хотя их масса невелика, они синтезируют тем не менее все биополимеры, из которых состоит матрикс — коллаген, эластин, протеогликоны, гликопротеины, и т.д. При удельном весе от 1 до 10% общего объема хрящевой ткани хондроциты обеспечивают образование больших масс матрикса. Они контролируют также все катаболические реакции в хряще.
В чем причина низкой метаболической активности хряща? Только в одном — в малом количестве клеток (1-10%) в единице объема ткани. В пересчете на чистую клеточную массу уровень метаболизма хондроцитов ничуть не меньше, чем у других клеток организма. Особенно низким метаболизмом отличаются суставные хрящи и пульподные ядра межпозвонковых дисков. Именно эти структуры отличаются самым малым количеством хондроцитов (1% от общей массы хряща) и именно они хуже всех других восстанавливаются после повреждений.
Окислительные процессы в хряще протекают в основном анаэробным (бескислородным) путем. Так, например, хондроциты пульпозных ядер межпозвоновых дисков на 99% питаются анаэробно и лишь на 1% аэробно. В среднем же кислородные окисление в хрящевой ткани как минимум в 50 раз менее интенсивно, чем в обычных тканях организма. Анаэробный характер окисления в хондроцитах — это защитно-приспособительная реакция, сложившаяся в процессе эволюции. И это неудивительно, если учесть, что хрящ не имеет (глаиновый, фиброзный) или почти не имеет (эластический) кровоснабжения. Если начать введение кислорода в пространство, пограничное с хрящом, то диффузия в хрящ О2 не только не улучшает его трофику, но, наоборот, резко ухудшает ее.
Насколько низка метаболическая активность хряща, можно понять из следующего сравнения. Белковый состав печени полностью обновляется за 4(!) дня. Коллаген хрящей обновляется всего лишь на 50% за 10(!) лет. Поэтому становится понятным, что любая травма хрящевой ткани практически неизлечима, если только не принять специальных мер, направленных на увеличение числа хондроцитов, которые сформируют новый матрикс.
Регенерация хрящевой ткани как физиологическая, так и репаративная (восстановительная) напрямую зависит от гормонального фона и модулирующего действия тех или иных гормонов. Так, например, глюкокортикоидные гормоны угнетают анаболические реакции в хондроцитах, ингибируют синтез коллагена и протеогликанов, вызывают дефицит глауроновой кислоты в синовиальной жидкости и в матриксе. И это угнетающее действие глюкокортикоидов более выражено, если оно сочетается со сдавлением (компрессией) хряща. В принципе, в этом нет ничего удивительного, если учесть, что глюкокортикоиды подавляют гликолиз — анаэробное окисление глюкозы в хряще. Регенерация без энергетического обеспечения становится попросту невозможной. Инсулин стимулирует синтез коллагена в матриксе хрящевой ткани, однако эта стимуляция невелика и носит опосредованный характер.
Самым сильным фактором, стимулирующим как физиологический, так и репаративный синтез в хрящевой ткани является соматотропный гормон. Сродство хрящей к соматотропному гормону отсутствует как таковое. Однако под действием соматотропного гормона в печени образуется инсулиноподобный фактор роста (ИРФ-1), который и обладает собственно анаболическим действием на все ткани, включая хрящевую. Сам по себе гормон роста способен оказывать анаболическое действие на клетки лишь в том случае, если его концентрация в 2000 раз превышает физиологическую. Такое возможно только в пробирке и полностью исключается в реальной жизни. Применяя соматотропин с репаративной целью необходимо помнить, что его влияние на синтез ИРФ-1 возможно лишь в условиях нормальной работы печени, при отсутствии серьезных заболеваний, иначе ИРФ-1 просто не будет синтезироваться и введение соматотропина не даст никакого результата. Способность соматомедина усиливать регенерацию хрящевой ткани в 100 раз превышает эффект от введения в организм инсулина и тестостерона. ИРФ-1 — это единственный фактор, вызывающий деление (размножение) хондроцитов. Другие анаболические факторы организма (а их довольно много) такой способностью не обладают.
Гормоны щитовидной железы могут усиливать восстановление и физиологический рост хрящей, если применять их в малых количествах, близких к физиологическим. Тогда они оказывают анаболическое действие на все ткани организма. В средних и больших количествах гормоны щитовидной железы оказывают еще большее анаболическое действие, однако, при этом они вызывают энергетический дефицит (термогенный эффект) и усиление катаболизма.
Катаболизм при этом усиливается в большей степени, чем анаболизм и активность деструктивных процессов превышает активность синтетическую. Как бы не усиливался анаболизм при увеличении доз тирсоидных гормонов, катаболизм усиливается еще больше и об этом необходимо помнить.
Тиреокальцитонин — единственный гормон щитовидной железы, усиливающий восстановление и рост хрящевой ткани в любых количествах, но для этого его необходимо применять изолированно, отдельно от тироксина и трийедиронина — «основных» гормонов щитовидной железы.
Гормон паращитовидных желез (паратиреоидный гормон) обладает умеренно стимулирующим действием на регенерацию хряща.
Тестостерон — основной андроген организма умеренно стимулирует биосинтетические процессы в хрящах, а эстрогены — женские половые гормоны, наоборот, тормозят ее.
Анаболические стероиды обладают способностью вызывать регенерацию хряща в намного большей степени, нежели чистый тестостерон и это неудивительно, если учесть, что они обладают анаболическим действием в несколько раз превышающим анаболическое действие тестостерона.
Интересно, что матрикс — порождение хондроцитов — живет своей самостоятельной жизнью. Он способен модулировать действие различных гормонов на хондроциты, ослабляя, либо усиливая их действие. Воздействуя на матрикс, можно изменить состояние хондроцитов как в лучшую, так и в худшую сторону. Удаление части матрикса вызывает немедленную интенсификацию биосинтеза недостающих в нем макромолекул. Более того, одновременно усиливается пролиферация (разрастание) хондроцитов. Количественные изменения в матриксе способны вызвать их качественные изменения.
Длительное ограничение движений в суставе (гипсовая иммобилизация и др.) приводит к уменьшению массы хрящей. Причина на удивление проста: в неподвижном суставе отсутствует перемешивание синовиальной жидкости. При этом диффузия молекул в хрящевую ткань замедляется и питание хондроцитов ухудшается. Недостаток прямой компрессивной нагрузки (на сжатие) так же приводит к ухудшению питания хондроцитов. Хрящу нужна хотя бы минимальная компрессионная нагрузка для поддержания нормальной трофики. Чрезмерная нагрузка на растяжение в эксперименте вызывает перерождение хряща с развитием грубых фиброзных волокон.
Очень сложное влияние на состояние внутрисуставных хрящей оказывает синовиальная оболочка. Она может как усиливать анаболизм хрящевой ткани, так и усиливать ее катаболизм. Удаление синовиальной оболочки резко ухудшает трофику хрящей, которая восстанавливается лишь после ее отрастания.
Хондроциты способны и к ауторегуляции. Они синтезируют специальные факторы роста, стимулирующие разрастание соседних хондроцитов. Пока их структура полностью не расшифрована. Известно лишь то, что они имеют полипептидную природу.
Все хрящи, но особенно хрящи опорно-двигательного аппарата постоянно подвергаются микротравматизации. В первую очередь это относится к межпозвонковыми дисками, наиболее уязвимая часть которых — пульпозное ядро. Уже в подростковом возрасте (начиная с 16-ти лет) начинаются дистрофические изменения в межпозвонковых дисках шейного отдела позвоночника. В пересчете на единицу поперечного сечения он несет нагрузку намного большую, чем любой другой отдел позвоночника, включая поясничный. Прежде всего дистрофические изменения касаются пульпозного ядра. Часть его клеток гибнет и замещается грубой соединительной тканью. Аналогичные, но менее выраженные изменения происходят и в самом межпозвоночном диске. Местами происходит очаговое разрастание хондроцитов. Организм стремится восстановить поврежденный хрящ и запускает репаративные процессы. Однако в местах гибели хондроцитов находится грубоволокнистая соединительная ткань — своеобразный рубец. И как раз в нем, там где они необходимы, хондроциты восстановиться не могут. Их разрастание происходит по периферии рубцевой ткани, где они, собственно и не нужны. Это приводит к ненужной деформации хряща, что еще более нарушает его функции. Основная функция хряща — опорная и стабилизирующая. При развитии дегенеративных и дистрофических процессов в межпозвоновых дисках позвонки теряют стабильность и постепенно становятся гипермобильными, легко смещаемыми. Их гипермобильность может вызвать сдавление окружающих их мягких тканей. Отек мягких тканей, в свою очередь, вызывает сдавление проходящих в них сосудов и нервов с развитием соответствующих симптомов. Организм стремится восстановить стабильность суставно-связочного аппарата. Происходит разрастание отдельных участков позвонков в виде своеобразных костных выростов — «усов». Эти «усы» сдавливают близлежащие мягкие ткани, вызывая их отек и вторичное сдавливание близлежащих сосудов и нервов. Весь комплекс изменений костно-хрящевого аппарата в данном случае носит название остеохондроза, хотя термин этот очень расплывчатый, неконкретный, и вообще-то, малонаучный.
Если в шейном отделе позвоночника негативные явления развиваются с подросткового возраста, то в поясничном отделе, где нагрузка на единицу поперечного сечения намного ниже — начиная с 25-30 лет. В целом они носят такой же морфологический характер, как и в шейном отделе, но отличаются клиническими (медицинскими) признаками. В шейном отделе позвоночника сквозь поперечные отростки шейных позвонков проходят крупные артерии, питающие все основание мозга и его стволовую часть, где находится жизненно важные центры (дыхания, кровообращения и т.д.). С развитием шейного остеохондроза происходит постепенное незаметное сдавливание этих артерий с развитием недостаточности мозгового кровообращения. При этом практически не бывает (или они бывают очень редко) никаких болевых признаков процесса. В поясничном отделе позвоночника картина несколько иная. Из этого отдела выходят нервные корешки, несущие чувствительные волокна от нижних конечностей и двигательные волокна к мышцам ног. Поясничный остеохондроз прежде всего проявляется различными болевыми симптомами, нарушением чувствительности и двигательной сферы. При этом никаких жизненно важных функций организма он не нарушает. Шейный остеохондроз никакими болевыми признаками себя не обнаруживает и особых неудобств не доставляет, однако может привести к серьезным нарушениям мозгового кровообращения, вплоть до инсультов с развитием параличей.
Шейный остеохондроз проявляется самыми разными симптомами, которые могут симулировать другие заболевания. Ухудшение мозгового кровообращения проявляется снижением работоспособности, быстрой утомляемостью, головной болью. Усталость глаз, мушки перед глазами, ощущение «песка в глазах» являются характерными признаками шейного остеохондроза. Звон в ушах и ухудшение слуха чаще говорят о нарушениях мозгового кровообращения вследствие остеохондроза, чем о заболеваниях слухового аппарата. По последним данным, 85% всех кровоизлияний в мозг в позднем возрасте вызваны не возрастной патологией артерий как таковой, а сдавлением шейных артерий в результате распространенного шейного остеохондроза.
Возрастные изменения эластических хрящей не носят фатального характера. Они выражаются в основном в оссификации — накоплении кальция и не приводят ко сколько-нибудь заметному нарушению функций.
В глиаминовых хрящах суставов уже начиная с 30-летнего возраста обнаруживается фибриляция — разволокнение хрящевой поверхности. При микроскопическом исследовании на поверхности хряща обнаруживаются разломы и расщепления. Расщепление хряща происходит как вертикальном, так и в горизонтальном направлении. При этом местами встречаются скопление клеток хрящевой ткани как ответная реакция организма на разрушение хряща. Иногда отмечается возрастное увеличение (!) толщины суставных хрящей как ответное действие на действия механических (тренировка) факторов. Возрастную эволюцию хрящей коленного сустава многие исследователи отмечают начиная уже с 40-летнего возраста. Наиболее существенное изменение, отмечаемое при старении хряща — это уменьшение содержания воды, что автоматически приводит к снижению его прочности.
Отсюда чрезвычайная сложность его посттравматического лечения. Более того, иногда непросто бывает даже сохранение нормального состояния хрящей в ходе обычного тренировочного процесса. Рост мышечной ткани опережает упрочнение суставно-связочного аппарата и в особенности его хрящевой части. Поэтому, рано или поздно, нагрузки достигают такой величины, которую хрящевая часть опорно-двигательного аппарата уже не может выдержать. В результате возникают «неизбежные» труднозалечиваемые травмы, из-за которых спортсмен иногда расстается со спортом. Самостоятельное восстановление хряща никогда не бывает полным. В лучшем случае хрящ восстанавливается на 50% от исходной величины. Однако это не значит, что дальнейшее его восстановление невозможно. Оно возможно при грамотном фармакологическом воздействии, призванном вызвать, с одной стороны, размножение хондроцитов, а с другой — изменение состояния матрикса хряща. Проблема восстановления хряща многократно усложняется еще и тем, что на месте погибшей хрящевой ткани развивается рубцовая ткань. Она не дает хрящу регенерировать в нужном месте. Компенсаторное разрастание участков хряща по соседству с местом повреждения приводит к его деформации, затрудняя задачу фармакологической стимуляции роста. Впрочем, все эти сложности преодолимы, если деформированный хрящ вначале подвергнуть хирургической коррекции.
Потенциальные возможности регенерации хряща достаточно велики. Он может регенерировать за счет собственного потенциала (размножение хондроцитов и рост матрикса) и, что не менее важно, за счет других видов соединительной ткани, которые имеют общее с ним происхождение. Примыкающие к хрящу ткани обладают способностью к переориентации своих клеток и превращению их в хрящеподобную ткань, которая неплохо справляется со своими функциями. Возьмем для примера самый частый вид повреждений — повреждение внутрисуставного хряща.
Источником регенерации являются:
1) сам хрящ;
2) синовиальная оболочка сустава, нарастающая с краев дефекта и превращающаяся в хрящеподобную ткань;
3) костные клетки, которые, не будем забывать, имеют хрящевое происхождение и при необходимости могут трансформироваться «обратно» в ткань, напоминающую по своему строению хрящевую;
4) клетки костного мозга, которые могут служить источником регенерации при глубоких повреждениях хрящей в сочетании с костным повреждением.
Сразу же после травмы наблюдается «взрыв» митоической активности хондроцитов, которые размножаются и формируют новый матрикс. Процесс этот наблюдается в течение 2-х недель после повреждения, однако ремодулирование поверхности хряща длится не менее 6-и месяцев, а полностью прекращается лишь через год. Качество «нового» хряща, конечно же, уступает качеству «старого». Если, например, поврежден гиалиновый внутрисуставный хрящ, то через 3-6 месяцев вырастает регенерат, имеющий характер гиалиново-фиброзного молодого хряща, а через 8-12 месяцев, он уже превращается в типичный фиброзный хрящ с матриксом, состоящим из плотно прилегающих друг к другу коллагеновых волокон.
Все исследователи хрящевой ткани единодушны в одном: хрящ не способен восстановить утраченное только за счет собственных внутренних ресурсов и механизмов. Их хватает максимум на 50% регенерата. Еще некоторый прирост регенерата осуществляется за счет других видов соединительной ткани, о которых мы уже говорили, но о полном 100% восстановлении хряща говорить все равно не приходится. Все это вносит изрядную долю пессимизма в оценку возможности выздоровления после сколько-нибудь серьезной травмы хряща, однако поводы для оптимизма все-таки есть. Достижения фармакологии и трансплантологии на сегодняшний день таковы, что можно говорить о полной компенсации даже очень серьезных хрящевых дефектов, как бы ни было это трудоемко.
Полнота восстановления поврежденной хрящевой ткани во многом зависит от качества мероприятий посттравматического периода, когда еще только формируется гематома1. Потом она пропитывается особого рода белком — фибрином, пропотевающим из плазмы крови, и превращается в рубцовую ткань. А она, как мы знаем, является серьезным препятствием для развития именно в этом месте полноценного регенерата. Поэтому сразу же после травмы необходимо предпринять все возможные меры для предотвращения развития гематомы и отека мягких тканей. Травмированный участок надо охладить. Для этого его обкладывают льдом, орошают хлорэтиленом. Если поврежден сустав конечности, то его можно просто поместить под струю холодной воды. Очень важна своевременная помощь квалифицированного врача-травматолога. Местные новокаиновые блокады не только обезболивают травмированный участок, но и препятствуют развитию отека и воспаления. Блокады можно повторять до тех пор, пока не минует острый период. Если в результате ушиба сустава произошло кровоизлияние в его полость — гемартроз, то необходимо как можно скорее откачать кровь из сустава. Сделать это несложно обычным шприцем. Иногда откачивать кровь и транссудат (жидкость, пропотевающую в полость сустава из плазмы крови) приходится несколько раз подряд. Ни в коем случае нельзя ждать, пока кровь «рассосется сама». Сгусток крови в результате выпадения особого рода белка — фибрина может развиться большое количество рубцовой ткани. Поврежденный сустав может так и остаться деформированным и увеличенным в размерах. Печальным примером может служить «кентус» у тех, кто занимается каратэ. Разбитые суставы пальцев увеличиваются в размерах из-за кровоизлияний и так остаются увеличенными из-за того, что из них вовремя не откачивают кровь. Несмотря на устрашающий вид кулаки с разбитыми суставами намного слабее обычных и очень легко повреждаются по повторном травмировании.
В подостром периоде, когда отек мягких тканей и болевой синдром существенно снижены, необходимо позаботиться, чтобы как можно полнее рассосалась поврежденная ткань. С этой целью применяет протеолитические ферменты (трипсин, хелеотрипсин, папаин и др.), которые вводятся в поврежденный участок при помощи электрофореза. Хороший эффект дают глюкокортикоидные гормоны — гидрокортизон, преднизолон и др. Как и протеолитические ферменты они вводятся местно, в пораженную область — будь то межпозвоновый диск или суставы конечностей. Гидрокортизон вводят с помощью ультразвука, а преднизолон — электрофорезом. Иногда вводят глюкокортикоидные гормоны в полости суставов, например, при лечении травм коленного сустава. У него самое сложное строение и лечить его травмы весьма непросто. Мениски — внутрисуставные хрящи в коленных суставах при повреждениях практически не срастаются. Поэтому, если имеются надрывы или отрывы частей менисков их необходимо как можно раньше удалить. Легче «вырастить» регенерат на месте удаленного мениска (а такой регенерат обязательно вырастает), чем добиться заживления мениска поврежденного. К счастью, в последние годы широкое развитие получила артроскопия и операции на коленном суставе становятся все более и более щадящими. Артроскоп позволяет с помощью волокнистой оптики заглянуть внутрь сустава не вскрывая его (проделываются лишь несколько отверстий). Через артроскоп же проводится и оперативное вмешательство. Иногда бывает так, что в результате травмы мениск остается целым, но отрывается от места своего прикрепления. Если раньше такой мениск всегда удаляли, то теперь все больше появляется специалистов, которые пришивают оторванный мениск на место. После освежения краев раны пришитый мениск прирастает на место.
Если при артроскопии обнаруживается разволокнение тех или иных хрящевых поверхностей, то их шлифуют, «скусывают» специальными кусачками волокна и участки деформированного хряща. Если этого не сделать, то последующие меры, принятые для усиления регенерации хрящевой ткани могут привести к росту деформированного хряща и нарушению его опорных функций.
При поверхностных повреждениях можно добиться полного восстановления хряща применяя сильнодействующие фармакологические средства. За последние 40 лет экспериментальных и клинических работ свою высокую эффективность доказал лишь один единственный препарат — соматотропный гормон (СТГ). Он стимулирует рост хрящевой ткани в 100 раз сильнее, чем введение тестостерона и инсулина. Еще больший эффект оказывает комбинированное введение СТГ и тиреокальцитонина — особого рода гормона щитовидной железы, который усиливает репарацию как костной, так и хрящевой ткани. Исключительная эффективность действия СТГ на репарацию хряща обусловлено тем, что он стимулирует непосредственно деление хондроцитов. Используя СТГ теоретически можно довести количество хондроцитов до любого нужного количества. Они, в свою очередь, восстанавливают матрикс до необходимого объема, синтезируя все его компоненты, начиная с коллагеновых волокон и кончая протеогликанами. Недостатком СТГ является то, что его нельзя применять местно, вводя непосредственно в зону поражения хрящевой ткани, поскольку действует он опосредованно. СТГ вызывает образование в печени инсулиноподобного фактора роста (ИРФ-1) который и оказывает сильнейший анаболический эффект. Парентеральное (инъекционное) его введение вызывает рост не только поврежденных хрящей, но и нормальных тоже, а это нежелательно, ведь в организме существуют кости, в которых хрящевые зоны роста не закрываются на протяжении всей жизни. Длительное введение больших доз СТГ в сформировавшийся организм может вызвать диспропорции скелета. Хотя следует отметить, что на пораженный хрящ он действует сильнее, и явных деформаций скелета при лечении СТГ в научной литературе не встречается.
В последние годы синтезирована лекарственная формы ИРФ-1, которую все шире применяют инъекционно вместо соматотропина. Поскольку ИРФ-1 действует непосредственно на ткани (в т.ч. и на хрящевую), то возникает заманчивая перспектива использовать его для местного введения (электрофорез, ультразвук и т.д.). Такое применение ИРФ-1 позволило бы локализовать его действие местом пораженного хряща и исключить действие на здоровые хрящи организма.
Неплохое действие на восстановление хряща и окружающего его соединительной ткани оказывают анаболические стероиды (АС). По эффективности они стоят на втором месте после ИРФ-1 и соматотропного гормона, хотя непосредственно деления хондроцитов они не вызывают. Анаболические стероиды, однако, ускоряют физиологическую регенерацию и потенцируют анаболическое действие инсулина и других эндогенных анаболических факторов, блокируют действие катаболических гормонов (глюкокортикоидов). Практическое применение АС в хирургической и травматологической практике доказало их высокую эффективность. Очень жаль, что до сих пор не разработаны лекарственные формы АС для локального применения. Это позволило бы создавать высокие концентрации лекарственного вещества именно в месте повреждения и предотвращать системные (на уровне всего организма) побочные действия. К сожалению, исследования в данной сфере никем не финансируются из-за причисления АС к допинговым средствам в спорте.
Некоторые исследователи в области молекулярной биологии представили очень убедительный материал, доказывающий, что стимуляторы (2-адренергических рецепторов способны симулировать анаболические эффекты соматомединов и, в частности, по отношению к хрящевой ткани. Механизм такого действия не вполне ясен. Не исключено, что просто повышается чувствительность печени к эндогенному соматотропному гормону и возрастает синтез в печени ИРФ-1. Одним из наиболее сильных избирательных стимуляторов (2-адренергических рецепторов является кленбутерол. Этот препарат не обладает гормональными эффектами и, в то же время, оказывает хорошее анаболическое действие. Подобно ИРФ-1 он стимулирует рост хрящевой ткани и может с успехом применяться в посттравматическом восстановительном периоде. Препаратов, стимулирующих (2-адренорецепторы много, но особо хотелось бы отметить такое старое и проверенное средство как адреналин. Адреналин — гормон мозгового вещества надпочечников даже при длительном курсовом применении не вызывает привыкания. В больших дозах адреналин воздействует в основном на а-адренорецепторы. Происходит сужение сосудов кожи, повышение артериального давления, подъем уровня сахара в крови. Малые дозы адреналина не затрагивают а-адренорецепторов, стимулируют (2-адренорецепторы. Расширяются сосуды мышц, снижаются уровень сахара в крови и артериальное давление. Развивается общее анаболическое действие и, в особенности по отношению к хрящевой ткани. Ежедневное введение малых (именно малых!) доз адреналина хорошо зарекомендовало себя как средство, способствующее регенерации.
Некоторые витамины в больших фармакологических дозировках способны существенно увеличить выброс в кровь эндогенного соматотропина. Пальму первенства здесь держит никотиновая кислота (витамин РР). Внутривенное введение сравнительно небольших доз никотиновой кислоты способно увеличить базальную секрецию СТГ в 2-3 раза. Увеличивает секрецию гормона роста витамин К, только применять его необходимо в умеренных дозах, чтобы не повысить чрезмерно свертываемость крови.
Несмотря на то, что матрикс хрящевой ткани является производным хондроцитов, изменение его состояния может улучшить и их деятельность. Состояние матрикса можно улучшить, применяя большие дозы аскорбиновой кислоты в сочетании с витамином Р. Особенно сильно аскорбиновая кислота влияет на состоянии коллагеновых структур. Поэтому ее традиционно используют для усиления синтеза коллагена, особенно в сочетании с глицином и анаболическими стероидами. Применяется также сочетание больших доз аскорбиновой кислоты с лизином, аланином и пролином.
Состояние хрящевого матрикса внутрисуставных хрящей можно временно улучшить с помощью веществ, вводимых в синовиальную жидкость. В последние годы особенно широко используется введение в сустав 15% раствора поливинилпирролидона, где он пребывает приблизительно 5-6 дней, затем процедуру повторяют, иногда несколько раз. Поливинилпирролидон служит своеобразным временным «протезом» внутрисуставной жидкости. Он улучшает трение внутрисуставных поверхностей, временно снимая нагрузку с суставного хряща. В случаях тяжелых, необратимых повреждениях хрящевой ткани используется протезирование, которое по мере развития оперативной техники дает все более обнадеживающие результаты. Уже никого не удивишь протезами межпозвонковых дисков. Делаются небезуспешные попытки протезирования внутрисуставных хрящей (менисков) коленных суставов.
Очень перспективным направлением является введение в поврежденные участки взвеси хондроцитов. Слабая регенерация хрящевой ткани, как мы помним, обусловлена малым числом хрящевых клеток (хондроцитов) на единицу массы хрящевой ткани. Чужеродные хондроциты, будучи введенными, скажем, в полость сустава не вызывают реакции отторжения, т.к. обладают слабой иммунногенной активностью. Они способны размножаться и образовывать новую хрящевую ткань. Применяют взвесь хондроцитов, полученную из хрящей крупного рогатого скота, умерших людей. Наиболее перспективным представляется использование эмбриональных (зародышевых) хрящевых клеток. Они вообще не вызывают иммунного ответа и, размножаясь, вызывают образование новой хрящевой ткани. К сожалению, все работы с зародышевыми клетками носят пока экспериментальный характер и не вошли в широкую практику. Но это — дело недалекого будущего. Проблема репарации хрящевой ткани в скором времени должна быть решена. Для этого уже есть все предпосылки.
1 Прекращение роста большинства костей в длину могут служить признаком того, что уже возможно лечение, например, анаболическими стероидами, которые приводят к преждевременному закрытию ростовой зоны хряща, если ростовые зоны узе закрыты, (что явствует из рентгеновского снимка лучевой кости молодого человека), то уже отсутствует опасность слишком быстро закрыть зоны роста применения стероиды, а значит, их применение можно начинать.
1 Дословно это означает «кровяная опухоль», но термин не совсем соответствует сути явления. Гематома — это диффузно поврежденная ткань, набухшая от крови.
Из журнала «Muscle Nutrition Review» № 8
 Расположение хряща в организме n Хрящевые ткани выполняют формообразующую функцию у плода и опорную во взрослом организме. Хрящевую ткань можно встретить: n в области суставов (покрывая суставную поверхность относительно узким слоем), n в метафизах (т. е. между эпифизом и диафизом) трубчатых костей, n в межпозвонковых дисках, в передних отделах рёбер, в стенке дыхательных органов (гортани, трахеи, бронхов) и т. д.
Расположение хряща в организме n Хрящевые ткани выполняют формообразующую функцию у плода и опорную во взрослом организме. Хрящевую ткань можно встретить: n в области суставов (покрывая суставную поверхность относительно узким слоем), n в метафизах (т. е. между эпифизом и диафизом) трубчатых костей, n в межпозвонковых дисках, в передних отделах рёбер, в стенке дыхательных органов (гортани, трахеи, бронхов) и т. д.
 Развитие n Как и все прочие ткани внутренней среды организма, скелетные ткани развиваются n из мезенхимы (клетки которой, в свою очередь, выселяются из сомитов и спланхнотомов
Развитие n Как и все прочие ткани внутренней среды организма, скелетные ткани развиваются n из мезенхимы (клетки которой, в свою очередь, выселяются из сомитов и спланхнотомов
 Особенности n особая природа межклеточного вещество придаёт два важнейших свойства: n упругость и n прочность. n межклеточного вещества данных тканей. n Во многих случаях хрящ покрыт надхрящницей - волокнистой соединительной тканью, которая участвует в росте и питании хряща.
Особенности n особая природа межклеточного вещество придаёт два важнейших свойства: n упругость и n прочность. n межклеточного вещества данных тканей. n Во многих случаях хрящ покрыт надхрящницей - волокнистой соединительной тканью, которая участвует в росте и питании хряща.
 Важная особенность хрящевых тканей - - отсутствие кровеносных сосудов. Поэтому питательные вещества поступают в хрящ - путём диффузии из сосудов надхрящницы В ряде случае надхрящницы нет - например, у суставных хрящей, поскольку их поверхность должна быть гладкой. Здесь питание осуществляется со стороны синовиальной жидкости и со стороны подлежащей кости.
Важная особенность хрящевых тканей - - отсутствие кровеносных сосудов. Поэтому питательные вещества поступают в хрящ - путём диффузии из сосудов надхрящницы В ряде случае надхрящницы нет - например, у суставных хрящей, поскольку их поверхность должна быть гладкой. Здесь питание осуществляется со стороны синовиальной жидкости и со стороны подлежащей кости.
 Клеточный состав n Хондробласты – молодые клетки, располагаются в глубоких слоях надхрящницы по одиночке и расположены ближе к поверхности хряща n -небольшие уплощённые клетки, способные к -пролиферации и -синтезу компонентов межклеточного вещества хряща. n в них хорошо выражены ЭПС гранулярный, комплекс Гольджи, митохондрии n Хондробласты, выделяя компоненты межклеточного вещества, -"замуровывают" себя в нём и превращаются в хондроциты.
Клеточный состав n Хондробласты – молодые клетки, располагаются в глубоких слоях надхрящницы по одиночке и расположены ближе к поверхности хряща n -небольшие уплощённые клетки, способные к -пролиферации и -синтезу компонентов межклеточного вещества хряща. n в них хорошо выражены ЭПС гранулярный, комплекс Гольджи, митохондрии n Хондробласты, выделяя компоненты межклеточного вещества, -"замуровывают" себя в нём и превращаются в хондроциты.
 Функции n основная функция хондробластов - выработка органической части межклеточного вещества: белки коллаген и эластин, гликозаминогликаны (ГАГ) и протеогликаны (ПГ). n хондробласты обеспечивают аппозиционный (поверхностный) рост хряща со стороны надхрящницы.
Функции n основная функция хондробластов - выработка органической части межклеточного вещества: белки коллаген и эластин, гликозаминогликаны (ГАГ) и протеогликаны (ПГ). n хондробласты обеспечивают аппозиционный (поверхностный) рост хряща со стороны надхрящницы.
 Хондроциты n а) Хондроциты - главный тип клеток хряща. n -лежат в особых полостях межклеточного вещества (лакунах) и n - могут делиться митозом, при этом дочерние клетки не расходятся, остаются вместе - образуются изогенные группы (из 2 -6 клеток), происходящие из одной клетки. n б) Они имеют n -больший (по сравнению с хондробластами) размер и овальную форму. n Хорошо развиты гранулярная ЭПС и комплекс Гольджи
Хондроциты n а) Хондроциты - главный тип клеток хряща. n -лежат в особых полостях межклеточного вещества (лакунах) и n - могут делиться митозом, при этом дочерние клетки не расходятся, остаются вместе - образуются изогенные группы (из 2 -6 клеток), происходящие из одной клетки. n б) Они имеют n -больший (по сравнению с хондробластами) размер и овальную форму. n Хорошо развиты гранулярная ЭПС и комплекс Гольджи
 Функции n Хондроциты, прекратившие деление, активно синтезируют компоненты межклеточного вещества. n За счёт деятельности хондроцитов происходит увеличение массы хряща изнутри - интерстициальный рост.
Функции n Хондроциты, прекратившие деление, активно синтезируют компоненты межклеточного вещества. n За счёт деятельности хондроцитов происходит увеличение массы хряща изнутри - интерстициальный рост.
 Хондрокласты n В хрящевой ткани кроме клеток образующих межклеточное вещество есть и их антогонисты - разрушители межклеточного вещества - это хондрокласты (можно отнести к макрофагической системе): довольно крупные клетки, в цитоплазме много лизосом и митохондрий. Функция - разрушение поврежденных или изношенных участков хряща.
Хондрокласты n В хрящевой ткани кроме клеток образующих межклеточное вещество есть и их антогонисты - разрушители межклеточного вещества - это хондрокласты (можно отнести к макрофагической системе): довольно крупные клетки, в цитоплазме много лизосом и митохондрий. Функция - разрушение поврежденных или изношенных участков хряща.
 Межклеточное вещество n Межклеточное вещество хрящевой ткани содержит волокна и основное вещество. n много волокнистых структур: n -коллагеновых волокон, n а в эластическом хряще - эластических волокон.
Межклеточное вещество n Межклеточное вещество хрящевой ткани содержит волокна и основное вещество. n много волокнистых структур: n -коллагеновых волокон, n а в эластическом хряще - эластических волокон.
 n Межклеточное вещество обладает высокой гидрофильностью, содержание воды доходит до 75% массы хряща, это обуславливает высокую плотность и тургор хряща. Хрящевые ткани в глубоких слоях не имеют кровеносных сосудов,
n Межклеточное вещество обладает высокой гидрофильностью, содержание воды доходит до 75% массы хряща, это обуславливает высокую плотность и тургор хряща. Хрящевые ткани в глубоких слоях не имеют кровеносных сосудов,
 n Основное аморфное вещество содержит: n -воду (70 -80 %), -минеральные вещества (4 -7 %), -органический компонент (10 -15 %), представленный n -протеогликанами и -гликопротеинами.
n Основное аморфное вещество содержит: n -воду (70 -80 %), -минеральные вещества (4 -7 %), -органический компонент (10 -15 %), представленный n -протеогликанами и -гликопротеинами.
 Протеогликаны n Протеогликановый агрегат содержит 4 компонента. n В основе агрегата - длинная нить гиалуроновой кислоты (1). n С помощью глобулярных связующих белков (2) с этой нитью связаны n линейные (фибриллярные) пептидные цепи т. н. корового (сердцевинного) белка (3). n В свою очередь, от последних отходят олигосахаридные ветви (4).
Протеогликаны n Протеогликановый агрегат содержит 4 компонента. n В основе агрегата - длинная нить гиалуроновой кислоты (1). n С помощью глобулярных связующих белков (2) с этой нитью связаны n линейные (фибриллярные) пептидные цепи т. н. корового (сердцевинного) белка (3). n В свою очередь, от последних отходят олигосахаридные ветви (4).
 Эти комплексы n обладают высокой гидрофильностью; поэтому связывают большое количество воды и n обеспечивают высокую упругость хряща. n При этом они сохраняют проницаемость для низкомолекулярных метаболитов.
Эти комплексы n обладают высокой гидрофильностью; поэтому связывают большое количество воды и n обеспечивают высокую упругость хряща. n При этом они сохраняют проницаемость для низкомолекулярных метаболитов.
 n Надхрящница - это слой соединительной ткани, покрывающий поверхность хряща. В надхрящнице выделяют наружный фиброзный (из плотной неоформленной СТ с большим количеством кровеносных сосудов) и внутренний клеточный слой, содержащее большое количестволовых, полустволовых клеток.
n Надхрящница - это слой соединительной ткани, покрывающий поверхность хряща. В надхрящнице выделяют наружный фиброзный (из плотной неоформленной СТ с большим количеством кровеносных сосудов) и внутренний клеточный слой, содержащее большое количестволовых, полустволовых клеток.

 Гиалиновый хрящ n Внешне эта ткань имеет голубовато-белый цвет и похожа на стекло (греч. hyalos - стекло). Гиалиновый хрящ - покрывает все суставные поверхности костей, содержится в грудинных концах ребер, в воздухоносных путях.
Гиалиновый хрящ n Внешне эта ткань имеет голубовато-белый цвет и похожа на стекло (греч. hyalos - стекло). Гиалиновый хрящ - покрывает все суставные поверхности костей, содержится в грудинных концах ребер, в воздухоносных путях.
 Отличительные признаки n 1. межклеточное вещество гиалинового хряща в препаратах окрашенных гематоксилин-эозином кажется гомогенным, не содержащим волокон. n 2. вокруг изогенных групп имеется четко выраженная базофильная зона - так называемый территориальный матрикс. Это связано с тем, что хондроциты выделяют в большом количестве ГАГ с кислой реакцией, поэтому этот участок окрашивается основными красками, т. е. базофильна. Слабооксифильные участки между территориальными матриксами называются интертерриториальным матриксом. n
Отличительные признаки n 1. межклеточное вещество гиалинового хряща в препаратах окрашенных гематоксилин-эозином кажется гомогенным, не содержащим волокон. n 2. вокруг изогенных групп имеется четко выраженная базофильная зона - так называемый территориальный матрикс. Это связано с тем, что хондроциты выделяют в большом количестве ГАГ с кислой реакцией, поэтому этот участок окрашивается основными красками, т. е. базофильна. Слабооксифильные участки между территориальными матриксами называются интертерриториальным матриксом. n
 n Большое количество протеогликановых агрегатов. n Гликозаминогликаны. Высокая упругость зависит от содержания ГАГ n Хондроитинсульфаты (хондроитин-6 -сульфат, хондроитин-4 -сульфат) n Кератансульфаты n содержится коллаген II типа, который является более гидрофильным (за счёт более высокого содержания гидроксигрупп) и n образует лишь фибриллы (не объединяющиеся в волокна). n Коллаген IX, VI и Х n Белок хондронектин
n Большое количество протеогликановых агрегатов. n Гликозаминогликаны. Высокая упругость зависит от содержания ГАГ n Хондроитинсульфаты (хондроитин-6 -сульфат, хондроитин-4 -сульфат) n Кератансульфаты n содержится коллаген II типа, который является более гидрофильным (за счёт более высокого содержания гидроксигрупп) и n образует лишь фибриллы (не объединяющиеся в волокна). n Коллаген IX, VI и Х n Белок хондронектин
 Клеточный состав n а) Сразу под надхрящницей располагаются n молодые хондроциты (3) - n по несколько крупнее по размерам и более овальные по форме. n б) Глубже находятся n зрелые хондроциты n крупные овальные клетки со светлой цитоплазмой, n образующие изогенные группы (4) по 2 -6 клеток.
Клеточный состав n а) Сразу под надхрящницей располагаются n молодые хондроциты (3) - n по несколько крупнее по размерам и более овальные по форме. n б) Глубже находятся n зрелые хондроциты n крупные овальные клетки со светлой цитоплазмой, n образующие изогенные группы (4) по 2 -6 клеток.
 n 1) Суставные поверхности костей. n 2) Воздухоносные пути. n 3) Места соединения рёбер с грудиной.
n 1) Суставные поверхности костей. n 2) Воздухоносные пути. n 3) Места соединения рёбер с грудиной.
 Эластический хрящ n В ушной раковине, надгортаннике, хрящах гортани. В межклеточном веществе кроме коллагеновых волокон имеется большое количество беспорядочно расположенных эластических волокон, что придает эластичность хрящу. В эластическом хряще меньше содержание липидов, хондроитинсульфатов и гликогена.
Эластический хрящ n В ушной раковине, надгортаннике, хрящах гортани. В межклеточном веществе кроме коллагеновых волокон имеется большое количество беспорядочно расположенных эластических волокон, что придает эластичность хрящу. В эластическом хряще меньше содержание липидов, хондроитинсульфатов и гликогена.
 n б) в толще хрящевой пластинки - изогенные группы хондроцитов, n крупные, овальные и n имеют светлую цитоплазму. n Группы хондроцитов обычно имеют n вид цепочек (из 2 -х, реже большего числа клеток), ориентированы перпендикулярно к поверхности.
n б) в толще хрящевой пластинки - изогенные группы хондроцитов, n крупные, овальные и n имеют светлую цитоплазму. n Группы хондроцитов обычно имеют n вид цепочек (из 2 -х, реже большего числа клеток), ориентированы перпендикулярно к поверхности.
 Возрастные изменения n Из-за относительно низкого содержания коллагеновых фибрилл и отсутствия коллагена Х, в эластическом хряще n не происходит отложение солей кальция (обызвествление) при нарушении питания.
Возрастные изменения n Из-за относительно низкого содержания коллагеновых фибрилл и отсутствия коллагена Х, в эластическом хряще n не происходит отложение солей кальция (обызвествление) при нарушении питания.
 Волокнистый хрящ n Волокнистый хрящ расположен в местах прикрепления сухожилий к костям и хрящам, межпозвоночных дисках. По строению занимает промежуточное положение между плотной оформленной соединительной и хрящевой тканью. n
Волокнистый хрящ n Волокнистый хрящ расположен в местах прикрепления сухожилий к костям и хрящам, межпозвоночных дисках. По строению занимает промежуточное положение между плотной оформленной соединительной и хрящевой тканью. n
 n В межклеточном веществе гораздо больше коллагеновых волокон, расположенных ориентированно - образуют толстые пучки, хорошо видимые под микроскопом. Хондроциты чаще лежат по одиночке вдоль волокон, не образуя изогенные группы. Имеют вытянутую форму, палочковидное ядро и узкий ободок цитоплазмы.
n В межклеточном веществе гораздо больше коллагеновых волокон, расположенных ориентированно - образуют толстые пучки, хорошо видимые под микроскопом. Хондроциты чаще лежат по одиночке вдоль волокон, не образуя изогенные группы. Имеют вытянутую форму, палочковидное ядро и узкий ободок цитоплазмы.
 n На периферии волокнистый хрящ постепенно переходит n в плотную оформленную соединительную коллагеновые волокна которой приобретают ориентацию и идут от одного позвонка к другому. ткань, косую n б) В центральной части диска волокнистый хрящ переходит в пульпозное ядро, которое содержит гиалиновый хрящ, коллаген II типа (в виде фибрилл)
n На периферии волокнистый хрящ постепенно переходит n в плотную оформленную соединительную коллагеновые волокна которой приобретают ориентацию и идут от одного позвонка к другому. ткань, косую n б) В центральной части диска волокнистый хрящ переходит в пульпозное ядро, которое содержит гиалиновый хрящ, коллаген II типа (в виде фибрилл)
 Регенерация хрящей n Гиалиновый – незначительна. В основном участвует надхрящница n Эластический - меньше подвержен дегенерации и не обызвествляется n Волокнистый – слабая регенерация, способен обызвествляться
Регенерация хрящей n Гиалиновый – незначительна. В основном участвует надхрящница n Эластический - меньше подвержен дегенерации и не обызвествляется n Волокнистый – слабая регенерация, способен обызвествляться

 Состав n Костные ткани состоят из клеток и межклеточного вещества. n К дифферону костной ткани относятся n 1. стволовые и полустволовые (остеогенные) клетки, n остеобласты, n остеоциты n 2. остеокласты.
Состав n Костные ткани состоят из клеток и межклеточного вещества. n К дифферону костной ткани относятся n 1. стволовые и полустволовые (остеогенные) клетки, n остеобласты, n остеоциты n 2. остеокласты.
 Остеобласты n Остеобласты являются наиболее функционально активными клеточными элементами дифферона при остеогистогенезе. Во взрослом организме источником клеток, поддерживающих популяцию остеобластов, являются клетки рассредоточенного камбия в остеогенном слое надкостницы, Остеобласты имеют кубическую или призматическую форму. Ядро расположено эксцентрично. Остеобласты - типичные активно синтезирующие и секретирующие клетки, секреция осуществляется всей поверхностью клетки. В клетке имеется хорошо развитая гранулярная эндоплазматическая сеть, заполняющая практически всю цитоплазму, множество свободных рибосом и полисом,
Остеобласты n Остеобласты являются наиболее функционально активными клеточными элементами дифферона при остеогистогенезе. Во взрослом организме источником клеток, поддерживающих популяцию остеобластов, являются клетки рассредоточенного камбия в остеогенном слое надкостницы, Остеобласты имеют кубическую или призматическую форму. Ядро расположено эксцентрично. Остеобласты - типичные активно синтезирующие и секретирующие клетки, секреция осуществляется всей поверхностью клетки. В клетке имеется хорошо развитая гранулярная эндоплазматическая сеть, заполняющая практически всю цитоплазму, множество свободных рибосом и полисом,
 Функции n секретируют коллаген I типа, щелочную фосфатазу, остеокальцин, остеопонтин, трансформирующие факторы роста, остеонектин, коллагеназу и др. n Высоко дифференцированные остеобласты характеризуются постепенным снижением активности щелочной фосфатазы, остеокальцина, остеопонтина и отсутствием пролиферативной активности.
Функции n секретируют коллаген I типа, щелочную фосфатазу, остеокальцин, остеопонтин, трансформирующие факторы роста, остеонектин, коллагеназу и др. n Высоко дифференцированные остеобласты характеризуются постепенным снижением активности щелочной фосфатазы, остеокальцина, остеопонтина и отсутствием пролиферативной активности.
 n Роль в минерализации органической основы костного матрикса. Процесс минерализации костного матрикса начинается с отложения аморфного фосфата кальция. Во внеклеточный матрикс катионы кальция попадают из кровотока, где находятся в связанном с белками состоянии. n В присутствии щелочной фосфатазы, синтезированной остеобластами, находящиеся в межклеточном веществе глицерофосфаты расщепляются с образованием фосфат-аниона. Избыток последнего приводит к локальному увеличению Са и Р до уровня, при котором фосфат кальция выпадает в осадок. Подавляющая фракция минерала кости находится в виде кристаллов гидроксиапатитов. Кристаллы образуются на коллагеновых волокнах костного матрикса. Последние имеют структурные особенности, способствующие этому процессу. Дело в том, что молекулы предшественника коллагена - тропоколлагена таким образом упакованы в волокно, что между окончанием одной и началом другой остается зазор, называемый зоной отверстий. Именно в этой зоне первоначально и откладывается костный минерал. В дальнейшем кристаллы начинают расти в обе стороны, и процесс охватывает все волокно
n Роль в минерализации органической основы костного матрикса. Процесс минерализации костного матрикса начинается с отложения аморфного фосфата кальция. Во внеклеточный матрикс катионы кальция попадают из кровотока, где находятся в связанном с белками состоянии. n В присутствии щелочной фосфатазы, синтезированной остеобластами, находящиеся в межклеточном веществе глицерофосфаты расщепляются с образованием фосфат-аниона. Избыток последнего приводит к локальному увеличению Са и Р до уровня, при котором фосфат кальция выпадает в осадок. Подавляющая фракция минерала кости находится в виде кристаллов гидроксиапатитов. Кристаллы образуются на коллагеновых волокнах костного матрикса. Последние имеют структурные особенности, способствующие этому процессу. Дело в том, что молекулы предшественника коллагена - тропоколлагена таким образом упакованы в волокно, что между окончанием одной и началом другой остается зазор, называемый зоной отверстий. Именно в этой зоне первоначально и откладывается костный минерал. В дальнейшем кристаллы начинают расти в обе стороны, и процесс охватывает все волокно
 n Существенная роль в минерализации синтезированного органического матрикса кости принадлежит матриксным пузырькам. Такие пузырьки являются производными комплекса Гольджи остеобластов, имеют мембранное строение и содержат различные ферменты, необходимые для реакций минерализации или их ингибирования, а также аморфные фосфаты кальция. Матриксные пузырьки выходят из клеток во внеклеточное пространство и высвобождают заключенные в них продукты. Последние инициируют процессы минерализации.
n Существенная роль в минерализации синтезированного органического матрикса кости принадлежит матриксным пузырькам. Такие пузырьки являются производными комплекса Гольджи остеобластов, имеют мембранное строение и содержат различные ферменты, необходимые для реакций минерализации или их ингибирования, а также аморфные фосфаты кальция. Матриксные пузырьки выходят из клеток во внеклеточное пространство и высвобождают заключенные в них продукты. Последние инициируют процессы минерализации.
 Остеоциты n По количественному составу самые многочисленные клетки костной ткани. Это отростчатые клетки, лежат в костных полостях - лакунах. Диаметр клеток достигает до 50 мкм. Цитоплазма слабобазофильна. Органоиды развиты слабо (гранулярный ЭПС, ПК и митохондрии). Не делятся. n Функция: принимают участие в физиологической регенерации костной ткани, вырабатывают органическую часть межклеточого вещества. n На остеобласты и остеоциты стимулирующее влияние оказывает гормон щитовидной железы кальцитонин - усиливается синтез органической части межклеточного вещества и усиливается отложение кальция, при этом концентрация кальция в крови снижается.
Остеоциты n По количественному составу самые многочисленные клетки костной ткани. Это отростчатые клетки, лежат в костных полостях - лакунах. Диаметр клеток достигает до 50 мкм. Цитоплазма слабобазофильна. Органоиды развиты слабо (гранулярный ЭПС, ПК и митохондрии). Не делятся. n Функция: принимают участие в физиологической регенерации костной ткани, вырабатывают органическую часть межклеточого вещества. n На остеобласты и остеоциты стимулирующее влияние оказывает гормон щитовидной железы кальцитонин - усиливается синтез органической части межклеточного вещества и усиливается отложение кальция, при этом концентрация кальция в крови снижается.


 Остеокласты n n n Специализированные макрофаги. Их диаметр достигает до 100 мкм. Различные компартменты остеокластов специализированы для выполнения определенных функций. базальная зона, в ней в составе многочисленных (5 - 20) ядер сосредоточен генетический аппарат клетки. светлая зона, непосредственно контактирующая с костным матриксом. Благодаря ей, остеокласт по всему периметру плотно адгезируется к кости, создавая изолированное пространство между собой и поверхностью минерализованного матрикса. Адгезия остеокласта обеспечивается за счет ряда рецепторов к компонентам матрикса, основными из которых являются рецепторы к витронектину. Избирательная проницаемость этого барьера позволяет создавать специфическую микросреду в зоне адгезии клетки. везикулярная зона содержит лизосомы. Через мембрану гофрированной каемки транспортируются ферменты, кислые субстанции, образуется угольная кислота Н 2 СО 3; угольная кислота растворяет соли кальция, растворенный кальций вымывается в кровь. осуществляющие деминерализацию и дезорганизацию костного матрикса, что приводит к формированию резорбционной (эрозионной) лакуны Хаушипа.
Остеокласты n n n Специализированные макрофаги. Их диаметр достигает до 100 мкм. Различные компартменты остеокластов специализированы для выполнения определенных функций. базальная зона, в ней в составе многочисленных (5 - 20) ядер сосредоточен генетический аппарат клетки. светлая зона, непосредственно контактирующая с костным матриксом. Благодаря ей, остеокласт по всему периметру плотно адгезируется к кости, создавая изолированное пространство между собой и поверхностью минерализованного матрикса. Адгезия остеокласта обеспечивается за счет ряда рецепторов к компонентам матрикса, основными из которых являются рецепторы к витронектину. Избирательная проницаемость этого барьера позволяет создавать специфическую микросреду в зоне адгезии клетки. везикулярная зона содержит лизосомы. Через мембрану гофрированной каемки транспортируются ферменты, кислые субстанции, образуется угольная кислота Н 2 СО 3; угольная кислота растворяет соли кальция, растворенный кальций вымывается в кровь. осуществляющие деминерализацию и дезорганизацию костного матрикса, что приводит к формированию резорбционной (эрозионной) лакуны Хаушипа.
 Остеокласты n остеокласты имеют много ядер и большой объем цитоплазмы; зона цитоплазмы, прилегающая к костной поверхности называется гофрированной каемкой, здесь много цитоплазматических выростов и лизосом функции - разрушение волокон и аморфного вещества кости
Остеокласты n остеокласты имеют много ядер и большой объем цитоплазмы; зона цитоплазмы, прилегающая к костной поверхности называется гофрированной каемкой, здесь много цитоплазматических выростов и лизосом функции - разрушение волокон и аморфного вещества кости
 n Толстые коллагеновые волокна, лишенные цементирующего вещества, создают вид "щеточной каемки" Лизосомальные ферменты осуществляют протеолиз коллагена и других белков матрикса. Продукты протеолиза удаляются из остеокластических лакун трансцеллюлярным транспортом. В целом процесс снижения р. Н в лакуне осуществляется двумя механизмами: путем экзоцитоза кислого содержимого вакуолей в лакуну и благодаря действию протонных насосов - Н+-АТФаз, локализованных в мембране гофрированной каемки. Источником для ионов водорода служит вода и диоксид углерода, являющиеся результатом митохондриальных реакций окисления.
n Толстые коллагеновые волокна, лишенные цементирующего вещества, создают вид "щеточной каемки" Лизосомальные ферменты осуществляют протеолиз коллагена и других белков матрикса. Продукты протеолиза удаляются из остеокластических лакун трансцеллюлярным транспортом. В целом процесс снижения р. Н в лакуне осуществляется двумя механизмами: путем экзоцитоза кислого содержимого вакуолей в лакуну и благодаря действию протонных насосов - Н+-АТФаз, локализованных в мембране гофрированной каемки. Источником для ионов водорода служит вода и диоксид углерода, являющиеся результатом митохондриальных реакций окисления.
 Межклеточное вещество n 1. Неорганическая часть матрикса В значительной части содержит кальций (35%) и фосфор (50%) (фосфорнокислые и углекислые соли кальция) главным образом, в виде кристаллов гидроксиапатита (Ca 10(PO 4)6(OH)2 · (3 · Ca(OH)2), n и немного - в аморфном состоянии, небольшое количество фосфата магния - составляют 70% межклеточного вещества. В плазме неорганический фосфор содержится в виде анионов НРО 4 -2 и Н 2 РО 4 -2. n n Соотношение органической и неорганической части межклеточного вещества зависит от возраста: у детей органической части несколько больше 30%, а неорганической части меньше 70%, поэтому у них кости менее прочные, но зато более гибкие (не ломкие); в пожилом возрасте, наоборот, доля неорганической части увеличивается, а органической части уменьшается, поэтому кости становятся более твердыми, но более ломкими. - присутствуют кровеносные сосуды:
Межклеточное вещество n 1. Неорганическая часть матрикса В значительной части содержит кальций (35%) и фосфор (50%) (фосфорнокислые и углекислые соли кальция) главным образом, в виде кристаллов гидроксиапатита (Ca 10(PO 4)6(OH)2 · (3 · Ca(OH)2), n и немного - в аморфном состоянии, небольшое количество фосфата магния - составляют 70% межклеточного вещества. В плазме неорганический фосфор содержится в виде анионов НРО 4 -2 и Н 2 РО 4 -2. n n Соотношение органической и неорганической части межклеточного вещества зависит от возраста: у детей органической части несколько больше 30%, а неорганической части меньше 70%, поэтому у них кости менее прочные, но зато более гибкие (не ломкие); в пожилом возрасте, наоборот, доля неорганической части увеличивается, а органической части уменьшается, поэтому кости становятся более твердыми, но более ломкими. - присутствуют кровеносные сосуды:
 Органическая часть костного матрикса Органическая часть межклеточного вещества представлена n коллагеновыми (коллаген I, Х, V типов) очень мало гликозаминогликанов и протеогликанов. n - гликопротеины (щелочная фосфатаза, остеонектин); n - протеогликаны (кислые полисахариды и гликозаминогликаны - хондроитин-4 - и хондроитин-6 сульфаты, дерматансульфат и кератансульфат.); n - факторы роста (фактор роста фибробластов, трансформирующие факторы роста, костные морфогенетические белки) - цитокины, выделяемые клетками костной ткани и крови, осуществляющие местную регуляцию остеогенеза.
Органическая часть костного матрикса Органическая часть межклеточного вещества представлена n коллагеновыми (коллаген I, Х, V типов) очень мало гликозаминогликанов и протеогликанов. n - гликопротеины (щелочная фосфатаза, остеонектин); n - протеогликаны (кислые полисахариды и гликозаминогликаны - хондроитин-4 - и хондроитин-6 сульфаты, дерматансульфат и кератансульфат.); n - факторы роста (фактор роста фибробластов, трансформирующие факторы роста, костные морфогенетические белки) - цитокины, выделяемые клетками костной ткани и крови, осуществляющие местную регуляцию остеогенеза.
 белки, осуществляющие адгезию клеток n Остеонектин - гликопротеин кости и дентина, имеет высокое сродство к коллагену I типа и к гидроксиапатиту, содержит Сасвязывающие домены. Поддерживает в присутствии коллагена концентрацию Са и Р. Предполагается, что белок участвует во взаимодействии клетки и матрикса. n Остеопонтин является главным компонентом белкового состава матрикса, в частности поверхностей раздела, где он и аккумулируется в виде плотного покрова, названного линиями цементации (lamina limitans). Благодаря своим физико-химическим свойствам регулирует кальцификацию матрикса, специфично участвует в адгезии клеток к матриксу или матрикса к матриксу. Продукция остеопонтина - одно из наиболее ранних проявлений активности остеобластов. n Остеокальцин (ОК) - небольшой белок (5800 Да, 49 аминокислот) в минерализованном матриксе кости, участвует в процессе кальцификации,
белки, осуществляющие адгезию клеток n Остеонектин - гликопротеин кости и дентина, имеет высокое сродство к коллагену I типа и к гидроксиапатиту, содержит Сасвязывающие домены. Поддерживает в присутствии коллагена концентрацию Са и Р. Предполагается, что белок участвует во взаимодействии клетки и матрикса. n Остеопонтин является главным компонентом белкового состава матрикса, в частности поверхностей раздела, где он и аккумулируется в виде плотного покрова, названного линиями цементации (lamina limitans). Благодаря своим физико-химическим свойствам регулирует кальцификацию матрикса, специфично участвует в адгезии клеток к матриксу или матрикса к матриксу. Продукция остеопонтина - одно из наиболее ранних проявлений активности остеобластов. n Остеокальцин (ОК) - небольшой белок (5800 Да, 49 аминокислот) в минерализованном матриксе кости, участвует в процессе кальцификации,
 Классификация n Различают трубчатые, плоские и смешанные кости. Диафизы трубчатых костей и кортикальные пластинки плоских и смешанных костей построены из пластинчатой костной ткани покрытой надкостницей или периостом. В периосте принято различать два слоя: наружный - волокнистый, состоящий преимущественно из волокнистой соединительной ткани; внутренний, прилегающий к поверхности кости - остеогенный, или камбиальный.
Классификация n Различают трубчатые, плоские и смешанные кости. Диафизы трубчатых костей и кортикальные пластинки плоских и смешанных костей построены из пластинчатой костной ткани покрытой надкостницей или периостом. В периосте принято различать два слоя: наружный - волокнистый, состоящий преимущественно из волокнистой соединительной ткани; внутренний, прилегающий к поверхности кости - остеогенный, или камбиальный.
 Виды костных тканей грубоволокнистая (ретикулофиброзная) пластинчатая (тонковолокнистая) Основная особенность Коллагеновые волокна образуют а) Костное вещество толстые пучки, идущие в разных (организовано в пластинки). направлениях. б) Причём, в пределах одной пластинки волокна имеют одинаковое направление, а в пределах соседних пластинок - разное. Локализация 1. Плоские кости эмбриона. 2. Бугорки костей; места заросших черепных швов. Почти все кости взрослого человека: плоские (лопатка, тазовые кости, кости черепа), губчатые (рёбра, грудина, позвонки) и трубчатые.
Виды костных тканей грубоволокнистая (ретикулофиброзная) пластинчатая (тонковолокнистая) Основная особенность Коллагеновые волокна образуют а) Костное вещество толстые пучки, идущие в разных (организовано в пластинки). направлениях. б) Причём, в пределах одной пластинки волокна имеют одинаковое направление, а в пределах соседних пластинок - разное. Локализация 1. Плоские кости эмбриона. 2. Бугорки костей; места заросших черепных швов. Почти все кости взрослого человека: плоские (лопатка, тазовые кости, кости черепа), губчатые (рёбра, грудина, позвонки) и трубчатые.

 Пластинчатая костная ткань может иметь губчатую и компактную организацию. Губчатое костное вещество Компактное костное вещество Локализация Из губчатого вещества состоят: эпифизы трубчатых костей, внутренний слой (примыкающий к костномозговому каналу) диафизов трубчатых костей, губчатые кости, внутренняя часть плоских костей. Компактную структуру имеют большая часть диафизов трубчатых костей и поверхностный слой плоских костей. Отличительная черта Губчатое вещество построено из бессосудистых костных перекладин (балок), между которыми находятся промежутки – костные ячейки. В компактном костном веществе практически нет промежутков: за счёт разрастания костной ткани вглубь ячеек, остаются лишь узкие пространства для сосудов – т. н. центральные каналы остеонов Костный мозг В ячейках губчатого вещества содержатся сосуды, питающие кость, и красный костный мозг - кроветворный орган. Костномозговая полость диафизов трубчатых костей у взрослых содержит жёлтый костный мозг - жировую ткань.
Пластинчатая костная ткань может иметь губчатую и компактную организацию. Губчатое костное вещество Компактное костное вещество Локализация Из губчатого вещества состоят: эпифизы трубчатых костей, внутренний слой (примыкающий к костномозговому каналу) диафизов трубчатых костей, губчатые кости, внутренняя часть плоских костей. Компактную структуру имеют большая часть диафизов трубчатых костей и поверхностный слой плоских костей. Отличительная черта Губчатое вещество построено из бессосудистых костных перекладин (балок), между которыми находятся промежутки – костные ячейки. В компактном костном веществе практически нет промежутков: за счёт разрастания костной ткани вглубь ячеек, остаются лишь узкие пространства для сосудов – т. н. центральные каналы остеонов Костный мозг В ячейках губчатого вещества содержатся сосуды, питающие кость, и красный костный мозг - кроветворный орган. Костномозговая полость диафизов трубчатых костей у взрослых содержит жёлтый костный мозг - жировую ткань.
 Строение Состоят из костных пластинок а) При этом пластинки губчатого вещества обычно ориентированы вдоль направления костных балок, а не вокруг сосудов, как в остеонах компактного вещества. б) в достаточно толстых балках остеоны могут встречаться. Единица строения костные пластинки. Состоят из костных пластинок В компактном же веществе имеются пластинки 3 -х типов: общие (генеральные) – окружают всю кость, остеонные - лежат концентрическими слоями вокруг сосуда, образуя т. н. остеоны; вставочные - находятся между остеонами. остеоны.
Строение Состоят из костных пластинок а) При этом пластинки губчатого вещества обычно ориентированы вдоль направления костных балок, а не вокруг сосудов, как в остеонах компактного вещества. б) в достаточно толстых балках остеоны могут встречаться. Единица строения костные пластинки. Состоят из костных пластинок В компактном же веществе имеются пластинки 3 -х типов: общие (генеральные) – окружают всю кость, остеонные - лежат концентрическими слоями вокруг сосуда, образуя т. н. остеоны; вставочные - находятся между остеонами. остеоны.
 Строение остеона-основной структурной единицы кости В центре каждого остеона - кровеносный сосуд (1), вокруг последнего – несколько концентрических слоёв костных пластинок (2), называемых остеонными. Остеоны отграничены резорбционной (спайной) линией (3). Между остеонами лежат вставочные костные пластинки (4), которые представляют собой остатки прежних генераций остеонов. костные пластинки включают клетки (остеоциты), коллагеновые волокна и основное вещество, богатое минеральными соединениями. волокна в межклеточном веществе неразличимы, а само межклеточное вещество имеет твёрдую консистенцию.
Строение остеона-основной структурной единицы кости В центре каждого остеона - кровеносный сосуд (1), вокруг последнего – несколько концентрических слоёв костных пластинок (2), называемых остеонными. Остеоны отграничены резорбционной (спайной) линией (3). Между остеонами лежат вставочные костные пластинки (4), которые представляют собой остатки прежних генераций остеонов. костные пластинки включают клетки (остеоциты), коллагеновые волокна и основное вещество, богатое минеральными соединениями. волокна в межклеточном веществе неразличимы, а само межклеточное вещество имеет твёрдую консистенцию.
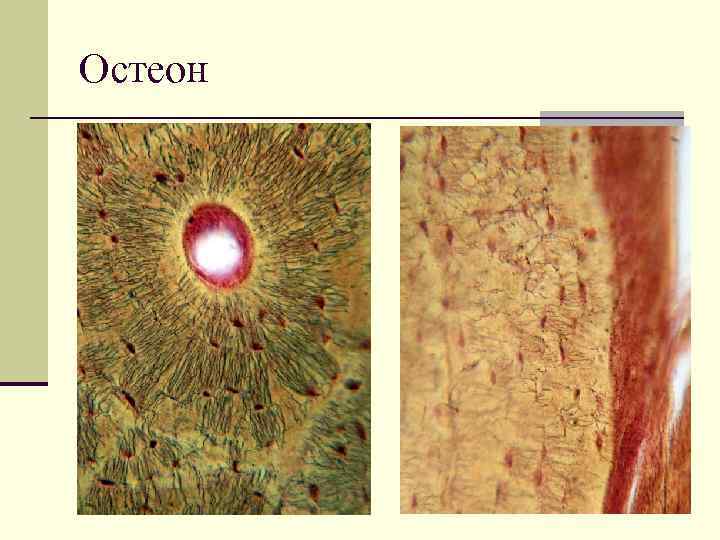
 Развитие КОСТИ ИЗ МЕЗЕНХИМЫ (прямой остеогистогенез). Из мезенхимы образуется незрелая (грубоволокнистая) кость, которая впоследствии замещается пластинчатой костью В развитии различают 4 этапа: n 1. образование остеогенного островка - в области образования кости клетки мезенхимы превращаются в остеобласты n
Развитие КОСТИ ИЗ МЕЗЕНХИМЫ (прямой остеогистогенез). Из мезенхимы образуется незрелая (грубоволокнистая) кость, которая впоследствии замещается пластинчатой костью В развитии различают 4 этапа: n 1. образование остеогенного островка - в области образования кости клетки мезенхимы превращаются в остеобласты n
 2. образованние межклеточного вещества n остеобласты начинают образовывать межклеточное вещество кости, при этом часть остеобластов оказывается внутри межклеточного вещества, эти остеобласты превращаются в остеоциты; другая часть остеобластов оказывается на поверхности межклеточного вещества,
2. образованние межклеточного вещества n остеобласты начинают образовывать межклеточное вещество кости, при этом часть остеобластов оказывается внутри межклеточного вещества, эти остеобласты превращаются в остеоциты; другая часть остеобластов оказывается на поверхности межклеточного вещества,
 3. кальцификация n межклеточного вещества кости межклеточное вещество пропитывается солями кальция. n а) На третьей стадии в межклеточном веществе появляются т. н. матриксные пузырьки, сходные с лизосомами. Они накапливают кальций и (за счёт щелочной фосфатазы) неорганический фосфат. n б) При разрыве пузырьков происходит минерализация межклеточного вещества, т. е. отложение кристаллов гидроксиапатита на волокнах и в аморфном веществе. В результате, образуются костные трабекулы (балки) - минерализованные участки ткани, содержащие все 3 типа костных клеток - n n n с поверхности - остеобласты и остеокласты, а в глубине - остеоциты.
3. кальцификация n межклеточного вещества кости межклеточное вещество пропитывается солями кальция. n а) На третьей стадии в межклеточном веществе появляются т. н. матриксные пузырьки, сходные с лизосомами. Они накапливают кальций и (за счёт щелочной фосфатазы) неорганический фосфат. n б) При разрыве пузырьков происходит минерализация межклеточного вещества, т. е. отложение кристаллов гидроксиапатита на волокнах и в аморфном веществе. В результате, образуются костные трабекулы (балки) - минерализованные участки ткани, содержащие все 3 типа костных клеток - n n n с поверхности - остеобласты и остеокласты, а в глубине - остеоциты.
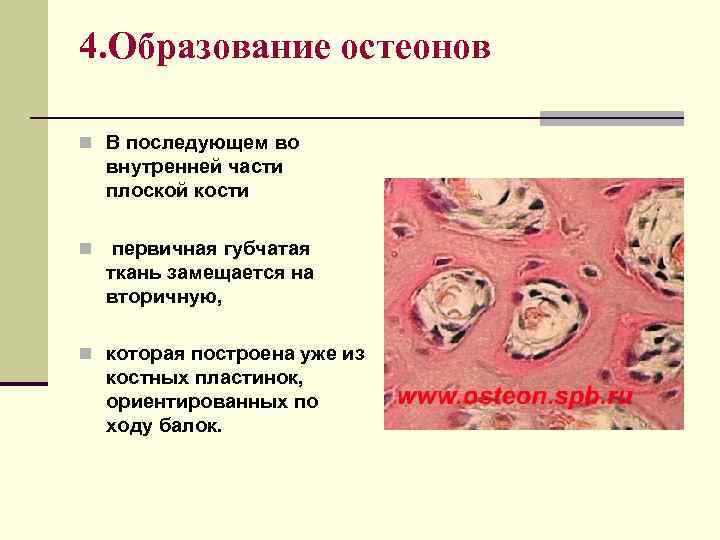 4. Образование остеонов n В последующем во внутренней части плоской кости n первичная губчатая ткань замещается на вторичную, n которая построена уже из костных пластинок, ориентированных по ходу балок.
4. Образование остеонов n В последующем во внутренней части плоской кости n первичная губчатая ткань замещается на вторичную, n которая построена уже из костных пластинок, ориентированных по ходу балок.
 Развитие пластинчатой костной ткани тесно связано с 1. процессом разрушения отдельных участков кости и врастанием кровеносных сосудов в толщу ретикулофиброзной кости. В этом процессе как в период эмбрионального остеогенеза, так и после рождения принимают участие остеокласты. 2. сосудами, подрастающие к трабекулам. В частности, вокруг сосудов костное вещество формируется в виде концентрических костных пластинок, составляющих первичные остеоны.
Развитие пластинчатой костной ткани тесно связано с 1. процессом разрушения отдельных участков кости и врастанием кровеносных сосудов в толщу ретикулофиброзной кости. В этом процессе как в период эмбрионального остеогенеза, так и после рождения принимают участие остеокласты. 2. сосудами, подрастающие к трабекулам. В частности, вокруг сосудов костное вещество формируется в виде концентрических костных пластинок, составляющих первичные остеоны.
 РАЗВИТИЕ КОСТИ НА МЕСТЕ ХРЯЩА (непрямой остеогенез) n на месте хряща сразу образуется зрелая (пластинчатая) кость n в развитии различают 4 этапа: n 1. образование хряща - на месте будущей кости образуется гиалиновый хрящ
РАЗВИТИЕ КОСТИ НА МЕСТЕ ХРЯЩА (непрямой остеогенез) n на месте хряща сразу образуется зрелая (пластинчатая) кость n в развитии различают 4 этапа: n 1. образование хряща - на месте будущей кости образуется гиалиновый хрящ
 2. перихондральное окостенение проходит только в области диафиза в области диафиза надхрящница превращается в надкостницу, в которой появляются остеогенные клетки, затем остеобласты за счет остеогенных клеток надкостницы на поверхности хряща начинается образование кости в виде общих пластинок, имеющих циркулярный ход, наподобие годовых колец дерева
2. перихондральное окостенение проходит только в области диафиза в области диафиза надхрящница превращается в надкостницу, в которой появляются остеогенные клетки, затем остеобласты за счет остеогенных клеток надкостницы на поверхности хряща начинается образование кости в виде общих пластинок, имеющих циркулярный ход, наподобие годовых колец дерева
 3. эндохондральное окостенение n Происходит как в области диафиза, так и в области эпифиза; внутрь хряща врастают кровеносные сосуды, где имеются остеогенные клетки - остеобласты, за счет которых вокруг сосудов происходит образование кости в виде остеонов, и остеокласты. n одновременно с образованием кости происходит разрушение хряща
3. эндохондральное окостенение n Происходит как в области диафиза, так и в области эпифиза; внутрь хряща врастают кровеносные сосуды, где имеются остеогенные клетки - остеобласты, за счет которых вокруг сосудов происходит образование кости в виде остеонов, и остеокласты. n одновременно с образованием кости происходит разрушение хряща
 зона пузырчатого хряща (4). На границе ещё сохранившегося хряща хрящевые клетки находятся в набухшем, вакуолизированном состоянии, т. е. имеют пузырчатую форму зона столбчатого хряща (5). В соседней области эпифиза продолжается рост хряща и, размножающиеся клетки выстраиваются в колонки вдоль длинной оси кости.
зона пузырчатого хряща (4). На границе ещё сохранившегося хряща хрящевые клетки находятся в набухшем, вакуолизированном состоянии, т. е. имеют пузырчатую форму зона столбчатого хряща (5). В соседней области эпифиза продолжается рост хряща и, размножающиеся клетки выстраиваются в колонки вдоль длинной оси кости.
 n а) В последующем произойдёт окостенение и самого эпифиза (за исключением суставной поверхности) - энхондральным путём. n б) Т. е. здесь тоже произойдёт минерализация, n сюда прорастут сосуды, разрушится вещество хряща и образуется вначале грубоволокнистая, n а потом пластинчатая костная ткань.
n а) В последующем произойдёт окостенение и самого эпифиза (за исключением суставной поверхности) - энхондральным путём. n б) Т. е. здесь тоже произойдёт минерализация, n сюда прорастут сосуды, разрушится вещество хряща и образуется вначале грубоволокнистая, n а потом пластинчатая костная ткань.
 n 4. перестройка и рост кости - старые участки кости постепенно разрушаются и на их месте образуются новые; за счет надкостницы образуются общие костные пластинки, за счет остеогенных клеток, находящихся в адвентиции сосудов кости, образуются остеоны. Между диафизом и эпифизом сохраняется прослойка хрящевой ткани, за счет котрой рост кости в длину продолжается до конца периода роста организма в длину, т. е. до 20 -21 года.
n 4. перестройка и рост кости - старые участки кости постепенно разрушаются и на их месте образуются новые; за счет надкостницы образуются общие костные пластинки, за счет остеогенных клеток, находящихся в адвентиции сосудов кости, образуются остеоны. Между диафизом и эпифизом сохраняется прослойка хрящевой ткани, за счет котрой рост кости в длину продолжается до конца периода роста организма в длину, т. е. до 20 -21 года.
 Рост кости Источники роста До 20 -летнего возраста происходит рост трубчатых костей: в ширину - путём аппозиционного роста со стороны надхрящницы, в длину - за счёт активности метаэпифизарной хрящевой пластинки. Метаэпифизарный хрящ а) Метаэпифизарная пластинка - часть эпифиза, примыкающая к диафизу и сохраняющая (в отличие от остальной части эпифиза) хрящевую структуру. б) В ней имеются 3 зоны (по направлению от эпифиза к диафизу): пограничная - содержит овальные хондроциты, зона столбчатых клеток - она-то и обеспечивает рост хряща в длину за счёт размножения хондроцитов, зона пузырчатого хряща - граничит с диафизом и подвергается окостенению. в) Таким образом, одновременно происходят 2 процесса рост хряща (в столбчатой зоне) и его замещение костью (в пузырчатой зоне).
Рост кости Источники роста До 20 -летнего возраста происходит рост трубчатых костей: в ширину - путём аппозиционного роста со стороны надхрящницы, в длину - за счёт активности метаэпифизарной хрящевой пластинки. Метаэпифизарный хрящ а) Метаэпифизарная пластинка - часть эпифиза, примыкающая к диафизу и сохраняющая (в отличие от остальной части эпифиза) хрящевую структуру. б) В ней имеются 3 зоны (по направлению от эпифиза к диафизу): пограничная - содержит овальные хондроциты, зона столбчатых клеток - она-то и обеспечивает рост хряща в длину за счёт размножения хондроцитов, зона пузырчатого хряща - граничит с диафизом и подвергается окостенению. в) Таким образом, одновременно происходят 2 процесса рост хряща (в столбчатой зоне) и его замещение костью (в пузырчатой зоне).
 Регенерация n Регенерация и рост кости в толщину осуществляется за счет периоста и эндоста. Все трубчатые кости, а также большинство плоских костей гистологически являются тонковолокнистой костью.
Регенерация n Регенерация и рост кости в толщину осуществляется за счет периоста и эндоста. Все трубчатые кости, а также большинство плоских костей гистологически являются тонковолокнистой костью.
 n В костной ткани постоянно происходят два противоположно направленных процесса - резорбция и новообразование. Соотношение этих процессов зависит от нескольких факторов, в том числе возраста. Перестройка костной ткани осуществляется в соответствии с действующими на кость нагрузками. n Процесс ремоделирования костной ткани происходит в несколько фаз, в каждую из которых ведущую роль выполняют те или иные клетки Первоначально участок костной ткани, подлежащий резорбции, "помечается" остеоцитами при помощи специфических цитокинов (активация). Разрушается протективный слой на костном матриксе. К оголенной поверхности кости мигрируют предшественники остеокластов, сливаются в многоядерную структуру - симпласт - зрелый остеокласт. На следующем этапе остеокласт деминерализует костный матрикс (резорбция), уступает место макрофагам, которые завершают разрушение органической матрицы межклеточного вещества кости и подготавливают поверхность к адгезии остеобластов (реверсия). На последнем этапе в зону разрушения прибывают предшественники, дифференцирующиеся в остеобласты, они синтезируют и минерализуют матрикс в соответствии с новыми условиями статической и динамической нагрузки на кость (формирование).
n В костной ткани постоянно происходят два противоположно направленных процесса - резорбция и новообразование. Соотношение этих процессов зависит от нескольких факторов, в том числе возраста. Перестройка костной ткани осуществляется в соответствии с действующими на кость нагрузками. n Процесс ремоделирования костной ткани происходит в несколько фаз, в каждую из которых ведущую роль выполняют те или иные клетки Первоначально участок костной ткани, подлежащий резорбции, "помечается" остеоцитами при помощи специфических цитокинов (активация). Разрушается протективный слой на костном матриксе. К оголенной поверхности кости мигрируют предшественники остеокластов, сливаются в многоядерную структуру - симпласт - зрелый остеокласт. На следующем этапе остеокласт деминерализует костный матрикс (резорбция), уступает место макрофагам, которые завершают разрушение органической матрицы межклеточного вещества кости и подготавливают поверхность к адгезии остеобластов (реверсия). На последнем этапе в зону разрушения прибывают предшественники, дифференцирующиеся в остеобласты, они синтезируют и минерализуют матрикс в соответствии с новыми условиями статической и динамической нагрузки на кость (формирование).



